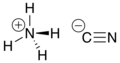Ó┤ģÓ┤«ÓĄŗÓ┤ŻÓ┤┐Ó┤»Ó┤é Ó┤ĖÓ┤»Ó┤©ÓĄłÓ┤ĪÓĄŹ
Ó┤ĖÓĄŹÓ┤źÓ┤┐Ó┤░Ó┤żÓ┤»Ó┤┐Ó┤▓ÓĄŹÓ┤▓Ó┤ŠÓ┤żÓĄŹÓ┤ż Ó┤ÆÓ┤░ÓĄü Ó┤ģÓ┤ĢÓ┤ŠÓĄ╝Ó┤¼Ó┤ŻÓ┤┐Ó┤Ģ Ó┤ĖÓ┤»Ó┤©ÓĄłÓ┤ĪÓĄŹ Ó┤ĖÓ┤éÓ┤»ÓĄüÓ┤ĢÓĄŹÓ┤żÓ┤«Ó┤ŠÓ┤ŻÓĄŹ Ó┤ģÓ┤«ÓĄŗÓ┤ŻÓ┤┐Ó┤»Ó┤é Ó┤ĖÓ┤»Ó┤©ÓĄłÓ┤ĪÓĄŹ (Ammonium cyanide). Ó┤ćÓ┤żÓ┤┐Ó┤©ÓĄŹÓ┤▒ÓĄå Ó┤żÓ┤©ÓĄŹÓ┤«Ó┤ŠÓ┤żÓĄŹÓ┤░Ó┤Š Ó┤ĖÓĄéÓ┤żÓĄŹÓ┤░Ó┤é NH4CN. Ó┤ēÓ┤¬Ó┤»ÓĄŗÓ┤ŚÓ┤éÓ┤ĢÓ┤ŠÓĄ╝Ó┤¼Ó┤ŻÓ┤┐Ó┤Ģ Ó┤¬Ó┤”Ó┤ŠÓĄ╝Ó┤żÓĄŹÓ┤źÓ┤ÖÓĄŹÓ┤ÖÓĄŠ Ó┤©Ó┤┐ÓĄ╝Ó┤«ÓĄŹÓ┤«Ó┤┐Ó┤ĢÓĄŹÓ┤ĢÓ┤ŠÓ┤©Ó┤ŠÓ┤ŻÓĄŹ Ó┤ģÓ┤«ÓĄŗÓ┤ŻÓ┤┐Ó┤»Ó┤é Ó┤ĖÓ┤»Ó┤©ÓĄłÓ┤ĪÓĄŹ Ó┤¬ÓĄŖÓ┤żÓĄüÓ┤ĄÓĄć Ó┤ēÓ┤¬Ó┤»ÓĄŗÓ┤ŚÓ┤┐Ó┤ĢÓĄŹÓ┤ĢÓĄüÓ┤©ÓĄŹÓ┤©Ó┤żÓĄŹ. Ó┤ģÓ┤ĖÓĄŹÓ┤źÓ┤┐Ó┤░ Ó┤ĖÓ┤éÓ┤»ÓĄüÓ┤ĢÓĄŹÓ┤żÓ┤«Ó┤ŠÓ┤»Ó┤żÓ┤┐Ó┤©Ó┤ŠÓĄĮ, Ó┤ĄÓĄŹÓ┤»Ó┤ĄÓ┤ĖÓ┤ŠÓ┤»Ó┤┐Ó┤Ģ Ó┤åÓ┤ĄÓ┤ČÓĄŹÓ┤»Ó┤ÖÓĄŹÓ┤ÖÓĄŠÓ┤ĢÓĄŹÓ┤ĢÓ┤ŠÓ┤»Ó┤┐ Ó┤ĢÓ┤»Ó┤▒ÓĄŹÓ┤▒ÓĄüÓ┤«Ó┤żÓ┤┐ Ó┤ÜÓĄåÓ┤»ÓĄŹÓ┤»Ó┤ŠÓ┤▒Ó┤┐Ó┤▓ÓĄŹÓ┤▓. Ó┤©Ó┤┐ÓĄ╝Ó┤«ÓĄŹÓ┤«Ó┤ŠÓ┤ŻÓ┤éÓ┤żÓ┤ŠÓ┤┤ÓĄŹÓ┤©ÓĄŹÓ┤© Ó┤żÓ┤ŠÓ┤¬Ó┤©Ó┤┐Ó┤▓Ó┤»Ó┤┐ÓĄĮ, Ó┤╣ÓĄłÓ┤ĪÓĄŹÓ┤░Ó┤£ÓĄ╗ Ó┤ĖÓ┤»Ó┤©ÓĄłÓ┤ĪÓĄŹ Ó┤£Ó┤▓ÓĄĆÓ┤» Ó┤ģÓ┤«ÓĄŗÓ┤ŻÓ┤┐Ó┤»Ó┤»ÓĄüÓ┤«Ó┤ŠÓ┤»Ó┤┐ Ó┤¼Ó┤¼ÓĄŹÓ┤¼ÓĄŹŌĆīÓ┤│Ó┤┐Ó┤éÓ┤ŚÓĄŹŌĆī Ó┤©Ó┤¤Ó┤żÓĄŹÓ┤żÓ┤┐ Ó┤ģÓ┤«ÓĄŗÓ┤ŻÓ┤┐Ó┤»Ó┤é Ó┤ĖÓ┤»Ó┤©ÓĄłÓ┤ĪÓĄŹ Ó┤©Ó┤┐ÓĄ╝Ó┤«ÓĄŹÓ┤«Ó┤┐Ó┤ĢÓĄŹÓ┤ĢÓ┤ŠÓ┤é
Ó┤ĢÓ┤ŠÓĄĮÓ┤ĖÓĄŹÓ┤»Ó┤é Ó┤ĖÓ┤»Ó┤©ÓĄłÓ┤ĪÓĄŹ, Ó┤ģÓ┤«ÓĄŗÓ┤ŻÓ┤┐Ó┤»Ó┤é Ó┤ĢÓ┤ŠÓĄ╝Ó┤¼Ó┤ŻÓĄćÓ┤▒ÓĄŹÓ┤▒ÓĄŹ Ó┤ÄÓ┤©ÓĄŹÓ┤©Ó┤┐Ó┤Ą Ó┤żÓ┤«ÓĄŹÓ┤«Ó┤┐ÓĄĮ Ó┤¬ÓĄŹÓ┤░Ó┤ĄÓĄ╝Ó┤żÓĄŹÓ┤żÓ┤┐Ó┤¬ÓĄŹÓ┤¬Ó┤┐Ó┤ÜÓĄŹÓ┤ÜÓĄüÓ┤é Ó┤ģÓ┤«ÓĄŗÓ┤ŻÓ┤┐Ó┤»Ó┤é Ó┤ĖÓ┤»Ó┤©ÓĄłÓ┤ĪÓĄŹ Ó┤©Ó┤┐ÓĄ╝Ó┤«ÓĄŹÓ┤«Ó┤┐Ó┤ĢÓĄŹÓ┤ĢÓ┤ŠÓ┤é
Ó┤¬ÓĄŖÓ┤¤ÓĄŹÓ┤¤Ó┤ŠÓ┤ĖÓĄŹÓ┤»Ó┤é Ó┤ĖÓ┤»Ó┤©ÓĄłÓ┤ĪÓĄŹ Ó┤ģÓ┤▓ÓĄŹÓ┤▓ÓĄåÓ┤ÖÓĄŹÓ┤ĢÓ┤┐ÓĄĮ Ó┤¬ÓĄŖÓ┤¤ÓĄŹÓ┤¤Ó┤ŠÓ┤ĖÓĄŹÓ┤»Ó┤é Ó┤½ÓĄåÓ┤▒ÓĄŗÓ┤ĖÓ┤»Ó┤©ÓĄłÓ┤ĪÓĄŹ Ó┤ģÓ┤«ÓĄŗÓ┤ŻÓ┤┐Ó┤»Ó┤é Ó┤ĢÓĄŹÓ┤▓ÓĄŗÓ┤▒ÓĄłÓ┤ĪÓĄüÓ┤«Ó┤ŠÓ┤»Ó┤┐ Ó┤¬ÓĄŹÓ┤░Ó┤ĄÓĄ╝Ó┤żÓĄŹÓ┤żÓ┤┐Ó┤¬ÓĄŹÓ┤¬Ó┤┐Ó┤ÜÓĄŹÓ┤ÜÓĄŹ Ó┤▓Ó┤ŁÓ┤┐Ó┤ĢÓĄŹÓ┤ĢÓĄüÓ┤©ÓĄŹÓ┤© Ó┤ĄÓ┤ŠÓ┤żÓ┤ĢÓ┤é Ó┤¢Ó┤░ÓĄĆÓ┤ŁÓ┤ĄÓ┤┐Ó┤¬ÓĄŹÓ┤¬Ó┤┐Ó┤ÜÓĄŹÓ┤ÜÓĄŹ Ó┤ģÓ┤«ÓĄŗÓ┤ŻÓ┤┐Ó┤»Ó┤é Ó┤ĖÓ┤»Ó┤©ÓĄłÓ┤ĪÓĄŹ Ó┤ĢÓĄŹÓ┤░Ó┤┐Ó┤ĖÓĄŹÓ┤▒ÓĄŹÓ┤▒ÓĄĮ Ó┤żÓ┤»ÓĄŹÓ┤»Ó┤ŠÓ┤▒Ó┤ŠÓ┤ĢÓĄŹÓ┤ĢÓ┤ŠÓ┤é.
Ó┤░Ó┤ŠÓ┤ĖÓ┤¬ÓĄŹÓ┤░Ó┤ĄÓĄ╝Ó┤żÓĄŹÓ┤żÓ┤©Ó┤ÖÓĄŹÓ┤ÖÓĄŠÓ┤ģÓ┤«ÓĄŗÓ┤ŻÓ┤┐Ó┤»Ó┤é Ó┤ĖÓ┤»Ó┤©ÓĄłÓ┤ĪÓĄŹ Ó┤ĄÓ┤┐Ó┤śÓ┤¤Ó┤┐Ó┤ÜÓĄŹÓ┤ÜÓĄŹ Ó┤ģÓ┤«ÓĄŗÓ┤ŻÓ┤┐Ó┤», Ó┤╣ÓĄłÓ┤ĪÓĄŹÓ┤░Ó┤£ÓĄ╗ Ó┤ĖÓ┤»Ó┤©ÓĄłÓ┤ĪÓĄŹ Ó┤ÄÓ┤©ÓĄŹÓ┤©Ó┤┐Ó┤ĄÓ┤»ÓĄüÓ┤ŻÓĄŹÓ┤¤Ó┤ŠÓ┤ĢÓĄüÓ┤©ÓĄŹÓ┤©ÓĄü.
Ó┤▓ÓĄŗÓ┤╣Ó┤┐Ó┤» Ó┤▓Ó┤ĄÓ┤ŻÓ┤ÖÓĄŹÓ┤ÖÓ┤│ÓĄüÓ┤«Ó┤ŠÓ┤»Ó┤┐ Ó┤¬ÓĄŹÓ┤░Ó┤ĄÓĄ╝Ó┤żÓĄŹÓ┤żÓ┤┐Ó┤ĢÓĄŹÓ┤ĢÓĄüÓ┤©ÓĄŹÓ┤©ÓĄü. Ó┤ŚÓĄŹÓ┤▓Ó┤»ÓĄŗÓ┤ĢÓĄŹÓ┤ĖÓ┤ŠÓ┤▓ÓĄüÓ┤«Ó┤ŠÓ┤»Ó┤┐ Ó┤¬ÓĄŹÓ┤░Ó┤ĄÓĄ╝Ó┤żÓĄŹÓ┤żÓ┤┐Ó┤ÜÓĄŹÓ┤ÜÓĄŹ Ó┤ŚÓĄŹÓ┤▓ÓĄłÓ┤ĖÓĄĆÓĄ╗ (aminoacetic acid) Ó┤ēÓ┤ŻÓĄŹÓ┤¤Ó┤ŠÓ┤ĢÓĄüÓ┤©ÓĄŹÓ┤©ÓĄü.
Ó┤ĄÓ┤┐Ó┤ĘÓ┤éÓ┤«Ó┤ŠÓ┤░Ó┤Ģ Ó┤ĄÓ┤┐Ó┤ĘÓ┤«Ó┤ŠÓ┤ŻÓĄŹ Ó┤ģÓ┤«ÓĄŗÓ┤ŻÓ┤┐Ó┤»Ó┤é Ó┤ĖÓ┤»Ó┤©ÓĄłÓ┤ĪÓĄŹ. Ó┤ČÓ┤░ÓĄĆÓ┤░Ó┤żÓĄŹÓ┤żÓ┤┐Ó┤▓ÓĄåÓ┤żÓĄŹÓ┤żÓ┤┐Ó┤»Ó┤ŠÓĄĮ Ó┤«Ó┤░Ó┤ŻÓ┤é Ó┤ĖÓ┤éÓ┤ŁÓ┤ĄÓ┤┐Ó┤ĢÓĄŹÓ┤ĢÓ┤ŠÓ┤é. Ó┤▓Ó┤ĄÓ┤ŻÓ┤é Ó┤ĄÓ┤┐Ó┤śÓ┤¤Ó┤┐Ó┤ÜÓĄŹÓ┤ÜÓĄŹ Ó┤╣ÓĄłÓ┤ĪÓĄŹÓ┤░Ó┤£ÓĄ╗ Ó┤ĖÓ┤»Ó┤©ÓĄłÓ┤ĪÓĄŹ Ó┤ēÓ┤ŻÓĄŹÓ┤¤Ó┤ŠÓ┤ĄÓĄüÓ┤©ÓĄŹÓ┤©Ó┤żÓ┤┐Ó┤©Ó┤ŠÓĄĮ Ó┤ģÓ┤żÓĄüÓ┤é Ó┤ĢÓĄłÓ┤ĢÓ┤ŠÓ┤░ÓĄŹÓ┤»Ó┤é Ó┤ÜÓĄåÓ┤»ÓĄŹÓ┤»ÓĄüÓ┤©ÓĄŹÓ┤©Ó┤żÓĄŹ Ó┤ģÓ┤¬Ó┤ĢÓ┤¤Ó┤«Ó┤ŠÓ┤ŻÓĄŹ. Ó┤░Ó┤ŠÓ┤ĖÓ┤śÓ┤¤Ó┤ĢÓ┤éÓ┤śÓ┤¤Ó┤ĢÓ┤ÖÓĄŹÓ┤ÖÓĄŠ: H 9.15%, C 27.23%, N 63.55%. Ó┤ģÓ┤ĄÓ┤▓Ó┤éÓ┤¼Ó┤é
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Portal di Ensiklopedia Dunia