Ó┤ĖÓĄŗÓ┤ĪÓ┤┐Ó┤»Ó┤é Ó┤ĢÓ┤ŠÓĄ╝Ó┤¼Ó┤ŻÓĄćÓ┤▒ÓĄŹÓ┤▒ÓĄŹ
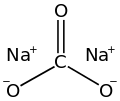
Sodium carbonate
Skeletal formula of sodium carbonate Space-filling model of sodium carbonate
Names
IUPAC name
Sodium carbonate
Other names
Soda ash, Washing soda, Soda crystals
Identifiers
ChEBI
ChEMBL
ChemSpider
ECHA InfoCard 100.007.127
EC Number
E number E500(i) (acidity regulators, ...)
RTECS number
UNII
InChI
SMILES
Properties
Na2 CO3
Molar mass
105.9888 g/mol (anhydrous)
Appearance
White solid, hygroscopic
Odor
Odorless
Ó┤ĖÓ┤ŠÓ┤©ÓĄŹÓ┤”ÓĄŹÓ┤░Ó┤ż
2.54 g/cm3 (25 ┬░C, anhydrous)3 (856 ┬░C)3 (monohydrate)[ 1] 3 (heptahydrate)3 (decahydrate)[ 2]
Ó┤”ÓĄŹÓ┤░Ó┤ĄÓ┤ŻÓ┤ŠÓ┤ÖÓĄŹÓ┤ĢÓ┤é
Decahydrate:[ 3]
Solubility
Soluble in aq. alkalis ,[ 3] glycerol alcohol CS2 , acetone , alkyl acetates , alcohol, benzonitrile , liquid ammonia [ 4]
Solubility in glycerine
98.3 g/100 g (15.5 ┬░C)[ 4]
Solubility in ethanediol
3.46 g/100 g (20 ┬░C)[ 5]
Solubility in dimethylformamide
0.5 g/kg[ 5]
Basicity (pK b )
3.67
ŌłÆ4.1┬Ę10ŌłÆ5 cm3 /mol[ 2]
1.485 (anhydrous)[ 6]
Ó┤ĄÓ┤┐Ó┤ĖÓĄŹÓ┤ĢÓĄŗÓ┤ĖÓ┤┐Ó┤▒ÓĄŹÓ┤▒Ó┤┐
3.4 cP (887 ┬░C)[ 5]
Structure
Monoclinic (╬│-form, ╬▓-form, ╬┤-form, anhydrous)[ 7] Orthorhombic (monohydrate, heptahydrate)[ 1] [ 8]
C2/m, No. 12 (╬│-form, anhydrous, 170 K)1 /n, No. 14 (╬┤-form, anhydrous, 110 K)[ 7] 1 , No. 29 (monohydrate)[ 1] [ 8]
2/m (╬│-form, ╬▓-form, ╬┤-form, anhydrous)[ 7] [ 1] [ 8]
a = 8.920(7) ├ģ,
b = 5.245(5) ├ģ,
c = 6.050(5) ├ģ (╬│-form, anhydrous, 295 K)
[ 7] ╬▒ = 90┬░, ╬▓ = 101.35(8)┬░, ╬│ = 90┬░
Octahedral (Na+ , anhydrous)
Thermochemistry
112.3 J/mol┬ĘK[ 2]
135 J/mol┬ĘK[ 2]
ŌłÆ1130.7 kJ/mol[ 2] [ 5]
ŌłÆ1044.4 kJ/mol[ 2]
Hazards
GHS labelling
[ 9]
Warning
H319 [ 9]
P305+P351+P338 [ 9]
NFPA 704
Lethal dose or concentration (LD, LC):
4090 mg/kg (rat, oral) [ 10]
Safety data sheet (SDS)
MSDS
Related compounds
Other anions
Sodium bicarbonate
Other cations
Lithium carbonate Potassium carbonate Rubidium carbonate Caesium carbonate
Except where otherwise noted, data are given for materials in their
standard state (at 25 ┬░C [77 ┬░F], 100 kPa).
Ó┤ĖÓĄŗÓ┤ĪÓ┤┐Ó┤»Ó┤é Ó┤ĢÓ┤ŠÓĄ╝Ó┤¼Ó┤ŻÓĄćÓ┤▒ÓĄŹÓ┤▒ÓĄŹ .(Ó┤ģÓ┤▓Ó┤ĢÓĄŹÓ┤ĢÓĄŹ Ó┤ĢÓ┤ŠÓ┤░Ó┤é,Ó┤ĄÓ┤ŠÓ┤ĘÓ┤┐Ó┤ÖÓĄŹ Ó┤ĖÓĄŗÓ┤Ī,Ó┤ĖÓĄŗÓ┤Ī Ó┤åÓ┤ĘÓĄŹ):ŌĆī-Ó┤ĢÓ┤ŠÓĄ╝Ó┤¼ÓĄŗÓ┤ŻÓ┤┐Ó┤ĢÓĄŹ Ó┤åÓ┤ĖÓ┤┐Ó┤ĪÓ┤┐Ó┤©ÓĄŹÓ┤▒ÓĄå Ó┤ĖÓĄŗÓ┤ĪÓ┤┐Ó┤»Ó┤é Ó┤▓Ó┤ĄÓ┤ŻÓ┤é.Ó┤░Ó┤ŠÓ┤Ė Ó┤ĖÓĄéÓ┤żÓĄŹÓ┤░Ó┤é Na2 CO3 . Ó┤£Ó┤▓Ó┤żÓĄŹÓ┤żÓ┤┐ÓĄĮ Ó┤©Ó┤©ÓĄŹÓ┤©Ó┤ŠÓ┤»Ó┤┐ Ó┤▓Ó┤»Ó┤┐Ó┤ĢÓĄŹÓ┤ĢÓĄüÓ┤©ÓĄŹÓ┤©ÓĄü. Ó┤¬ÓĄŹÓ┤░Ó┤ĢÓĄāÓ┤żÓ┤┐Ó┤»Ó┤┐ÓĄĮ Ó┤¬Ó┤░ÓĄĮ Ó┤░ÓĄéÓ┤¬Ó┤żÓĄŹÓ┤żÓ┤┐Ó┤▓ÓĄüÓ┤│ÓĄŹÓ┤│ Ó┤╣ÓĄåÓ┤¬ÓĄŹÓ┤▒ÓĄŹÓ┤▒Ó┤Š Ó┤╣ÓĄłÓ┤ĪÓĄŹÓ┤░ÓĄćÓ┤▒ÓĄŹÓ┤▒Ó┤ŠÓ┤»Ó┤┐ Ó┤ĢÓ┤ŠÓ┤ŻÓ┤¬ÓĄŹÓ┤¬ÓĄåÓ┤¤ÓĄüÓ┤©ÓĄŹÓ┤©ÓĄü.Ó┤ČÓĄüÓ┤”ÓĄŹÓ┤¦Ó┤«Ó┤ŠÓ┤» Ó┤ĖÓĄŗÓ┤ĪÓ┤┐Ó┤»Ó┤é Ó┤ĢÓ┤ŠÓĄ╝Ó┤¼Ó┤ŻÓĄćÓ┤▒ÓĄŹÓ┤▒ÓĄŹ Ó┤ĄÓĄåÓ┤│ÓĄüÓ┤żÓĄŹÓ┤ż Ó┤ŚÓ┤©ÓĄŹÓ┤¦Ó┤░Ó┤╣Ó┤┐Ó┤żÓ┤«Ó┤ŠÓ┤» Ó┤¬ÓĄŚÓ┤ĪÓ┤▒Ó┤ŠÓ┤ŻÓĄŹ. Ó┤ĢÓ┤¤ÓĄüÓ┤żÓĄŹÓ┤ż Ó┤ĢÓĄŹÓ┤ĘÓ┤ŠÓ┤░Ó┤░ÓĄüÓ┤ÜÓ┤┐Ó┤»ÓĄüÓ┤ŻÓĄŹÓ┤¤ÓĄŹ. Ó┤▓Ó┤ŠÓ┤»Ó┤┐Ó┤©Ó┤┐ Ó┤ĢÓĄŹÓ┤ĘÓ┤ŠÓ┤░ Ó┤ĖÓĄŹÓ┤ĄÓ┤ŁÓ┤ŠÓ┤ĄÓ┤«ÓĄüÓ┤│ÓĄŹÓ┤│Ó┤żÓ┤ŠÓ┤ŻÓĄŹ. Ó┤ŚÓ┤ŠÓ┤óÓ┤£Ó┤▓Ó┤żÓĄŹÓ┤żÓĄå Ó┤«ÓĄāÓ┤”ÓĄüÓ┤ĄÓ┤ŠÓ┤ĢÓĄŹÓ┤ĢÓ┤ŠÓĄ╗ Ó┤ĖÓ┤ŠÓ┤¦Ó┤ŠÓ┤░Ó┤ŻÓ┤»Ó┤ŠÓ┤»Ó┤┐ Ó┤ēÓ┤¬Ó┤»ÓĄŗÓ┤ŚÓ┤┐Ó┤ĢÓĄŹÓ┤ĢÓĄüÓ┤©ÓĄŹÓ┤©ÓĄü.
Ōåæ 1.0 1.1 1.2 1.3 Harper, J.P (1936). Antipov, Evgeny; Bismayer, Ulrich; Huppertz, Hubert; Petr├Łcek, V├Īclav; P├Čttgen, Rainer; Schmahl, Wolfgang; Tiekink, E.R.T.; Zou, Xiaodong (eds.). "Crystal Structure of Sodium Carbonate Monohydrate, Na2 CO3 . H2 O" . Zeitschrift f├╝r Kristallographie - Crystalline Materials . 95 (1). De Gruyter: 266ŌĆō 273. doi :10.1524/zkri.1936.95.1.266 . ISSN 2196-7105 . Retrieved 2014-07-25 . Ōåæ 2.0 2.1 2.2 2.3 2.4 2.5 2.6 Lide, David R., ed. (2009). CRC Handbook of Chemistry and Physics Boca Raton, Florida : CRC Press . ISBN 978-1-4200-9084-0 Ōåæ 3.0 3.1 Seidell, Atherton; Linke, William F. (1919). Solubilities of Inorganic and Organic Compounds New York : D. Van Nostrand Company. p. 633 . Ōåæ 4.0 4.1 Comey, Arthur Messinger; Hahn, Dorothy A. (February 1921). A Dictionary of Chemical Solubilities: Inorganic 208 ŌĆō209. Ōåæ 5.0 5.1 5.2 5.3 Anatolievich, Kiper Ruslan. "sodium carbonate" . http://chemister.ru the original on 2014-05-06. Retrieved 2014-07-25 . Ōåæ 6.0 6.1 Pradyot, Patnaik (2003). Handbook of Inorganic Chemicals . The McGraw-Hill Companies, Inc. p. 861. ISBN 0-07-049439-8 Ōåæ 7.0 7.1 7.2 7.3 Dusek, Michal; Chapuis, Gervais; Meyer, Mathias; Petricek, Vaclav (2003). "Sodium carbonate revisited" (PDF) . Acta Crystallographica Section B 59 (3). International Union of Crystallography: 337ŌĆō 352. doi :10.1107/S0108768103009017 . ISSN 0108-7681 . Retrieved 2014-07-25 . Ōåæ 8.0 8.1 8.2 Betzel, C.; Saenger, W.; Loewus, D. (1982). "Sodium Carbonate Heptahydrate". Acta Crystallographica Section B . 38 (11). International Union of Crystallography: 2802ŌĆō 2804. doi :10.1107/S0567740882009996 . Ōåæ 9.0 9.1 9.2 Sigma-Aldrich Co. , Sodium carbonate . Retrieved on 2014-05-06.Ōåæ http://chem.sis.nlm.nih.gov/chemidplus/rn/497-19-8 Ōåæ "Material Safety Data Sheet ŌĆō Sodium Carbonate, Anhydrous" (PDF) . http://www.conservationsupportsystems.com . Retrieved 2014-07-25 .