АмфотерністьАмфоте́рність — здатність сполук проявляти кислотні й основні властивості. Амфотерними сполуками (їх ще називають амфолітами) є вода, амінокислоти, гідроксиди алюмінію, цинку, хрому тощо. При дисоціації амфотерні сполуки дають іони Н+ і ОН−. Амфотерність багатьох сполук використовується в хімічному аналізі для розділення елементів. Амфотерні гідроксидиАмфотерні гідроксиди — речовини, до складу яких входить аніон ОН− (гідроксид-іон), і які при взаємодії з кислотами поводять себе як основи, а при взаємодії з основами — як кислоти. До амфотерних відносять гідроксиди, формально утворені від амфотерних оксидів: Zn(OH)2, Sn(OH)2, Pb(OH)2, Al(OH)3, Sn(OH)4, Pb(OH)4 тощо. Спрощене трактуванняФормули амфотерних гідроксидів у реакціях з кислотами слід записувати за типом основ, а в реакціях з основами — за типом кислот. В обох випадках утворюються солі. Наприклад: Точне трактуванняАмфотерні властивості, крім металічних елементів підгруп бору та карбону, більшою чи меншою мірою притаманні перехідним металам у їхніх нижчих та/або проміжних ступенях окиснення. Взаємодія амфотерних гідроксидів із розчинами лугів зумовлена утворенням гідроксильних комплексів, які відрізняються від продуктів сплавлення з лугами:
але при виділенні й нагріванні втрачають воду:
Амфотерні основи у розчині дисоціюють за осно́вним типом, з відщепленням OH–. Дисоціація амфотерних основ у водному розчині за кислотним типом, з відщепленням H+, гранично мала, нею завжди можна знехтувати. Оскільки стійкість гідроксильних комплексів не занадто висока, для повного розчинення амфотерного гідроксиду потрібно створити суттєву концентрацію лугу в розчині, тому в аналітичній хімії для розділення катіонів металів зазвичай застосовуються кращі методи. Органічні амфотерні сполуки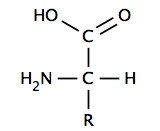 Найяскравішим прикладом є амінокислоти, молекули яких одночасно містять фрагменти з кислотною функцією (карбоксильна група –COOH) та з осно́вною функцією (аміногрупа –NH2). За певних умов можна побачити амфотерні властивості багатьох сполук, які зазвичай вважаються лише кислотою чи лише основою. Так, анілін Ph−NH2 у воді здатен приєднувати протон, тому традиційно класифікується як основа; але в рідкому аміаку він взаємодіє з амідом калію KNH2 як кислота: віддає протон з утворенням аніона Ph−NH− Див. такожПриміткиДжерела
|
Portal di Ensiklopedia Dunia














