Блок періодичної системи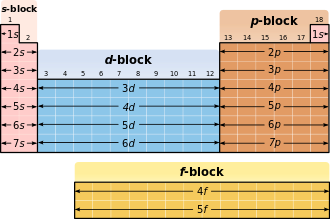 Блок періодичної таблиці — сукупність елементів періодичної таблиці з однаковими симетріями орбіталей валентних електронів. Уперше цей термін запровадив французький фізик Шарль Жане. Існують s-, p-, d- та f-блоки, гіпотетично g-блок. Така класифікація хімічних елементів іноді застосовується поряд зі звичною класифікацією за хімічними власитвостями. У ній Гідроген, Гелій, лужні метали та лужноземельні метали потрапляють в один s-блок, попри те, що Гелій — інертний газ. Електронна конфігураціяЕлектронна конфігурація — послідовність розташування електронів на різних електронних оболонках атома хімічного елемента:
Як показано в таблиці, електрони займають різні електронні орбіталі за фундаментальним принципом нарощування, який полягає в тому, що в основному стані атома, або іона, електрон спочатку займає енергетичний рівень з найменшою доступною енергією[2], яка визначається повним квантовим числом , де — головне квантове число, — азимутальне квантове число, яке визначає блок в структурі періодичної системи[3]. Період визначає ціла частина повниого квантового числоа . Наявність азимутального квантового числа призводить до того, що лише блоки s2 та p6 з'являються у своєму періоді, в той час, як блок d10 з'являється на один період пізніше, а блок f14 — на два.
Див. такожПримітки
Посилання |
Portal di Ensiklopedia Dunia

















