–ü–µ—Ä–µ–≥—Ä—ñ—Ç–∞ —Ä—ñ–¥–∏–Ω–∞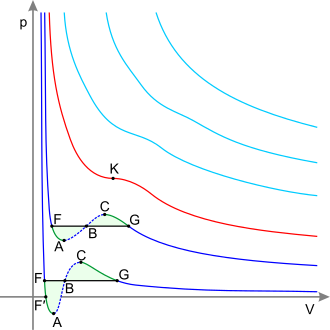 –õ—ñ–Ω—ñ—ó: –°–∏–Ω—ñ ‚Äî —ñ–∑–æ—Ç–µ—Ä–º–∏ –∑–∞ —Ç–µ–º–ø–µ—Ä–∞—Ç—É—Ä–∏ –Ω–∏–∂—á–æ—ó –≤—ñ–¥ –∫—Ä–∏—Ç–∏—á–Ω–æ—ó. –ó–µ–ª–µ–Ω—ñ –¥—ñ–ª—è–Ω–∫–∏ –Ω–∞ –Ω–∏—Ö ‚Äî –º–µ—Ç–∞—Å—Ç–∞–±—ñ–ª—å–Ω—ñ —Å—Ç–∞–Ω–∏. –ß–µ—Ä–≤–æ–Ω–∞ ‚Äî –∫—Ä–∏—Ç–∏—á–Ω–∞ —ñ–∑–æ—Ç–µ—Ä–º–∞. –ë–ª–∞–∫–∏—Ç–Ω—ñ ‚Äî –Ω–∞–¥–∫—Ä–∏—Ç–∏—á–Ω—ñ —ñ–∑–æ—Ç–µ—Ä–º–∏. –¢–æ—á–∫–∏: –¢–æ—á–∫–∞ F ‚Äî —Ç–æ—á–∫–∞ –∫–∏–ø—ñ–Ω–Ω—è. –¢–æ—á–∫–∞ K ‚Äî –∫—Ä–∏—Ç–∏—á–Ω–∞ —Ç–æ—á–∫–∞. –¢–æ—á–∫–∞ G ‚Äî —Ç–æ—á–∫–∞ —Ä–æ—Å–∏. –î—ñ–ª—è–Ω–∫–∏: –î—ñ–ª—è–Ω–∫–∞, —â–æ –ª–µ–∂–∏—Ç—å –ª—ñ–≤—ñ—à–µ –≤—ñ–¥ —Ç–æ—á–∫–∏ F ‚Äî –Ω–æ—Ä–º–∞–ª—å–Ω–∞ —Ä—ñ–¥–∏–Ω–∞. –ü—Ä—è–º–∞ FG ‚Äî —Ä—ñ–≤–Ω–æ–≤–∞–≥–∞ —Ä—ñ–¥–∫–æ—ó —ñ –≥–∞–∑–æ–ø–æ–¥—ñ–±–Ω–æ—ó —Ñ–∞–∑–∏. –î—ñ–ª—è–Ω–∫–∞ FA ‚Äî –ø–µ—Ä–µ–≥—Ä—ñ—Ç–∞ —Ä—ñ–¥–∏–Ω–∞. –î—ñ–ª—è–Ω–∫–∞ F‚Ä≤A ‚Äî —Ä–æ–∑—Ç—è–≥–Ω–µ–Ω–∞ —Ä—ñ–¥–∏–Ω–∞ (p<0) –î—ñ–ª—è–Ω–∫–∞ AC ‚Äî –∞–Ω–∞–ª—ñ—Ç–∏—á–Ω–µ –ø—Ä–æ–¥–æ–≤–∂–µ–Ω–Ω—è —ñ–∑–æ—Ç–µ—Ä–º–∏, —Ñ—ñ–∑–∏—á–Ω–æ –Ω–µ–º–æ–∂–ª–∏–≤–∏–π —Å—Ç–∞–Ω. –î—ñ–ª—è–Ω–∫–∞ CG ‚Äî –ø–µ—Ä–µ—Å–∏—á–µ–Ω–∞ (–ø–µ—Ä–µ–æ—Ö–æ–ª–æ–¥–∂–µ–Ω–∞) –ø–∞—Ä–∞. –î—ñ–ª—è–Ω–∫–∞, —â–æ –ª–µ–∂–∏—Ç—å –ø—Ä–∞–≤—ñ—à–µ –≤—ñ–¥ —Ç–æ—á–∫–∏ G ‚Äî –Ω–æ—Ä–º–∞–ª—å–Ω–∏–π –≥–∞–∑ (–ø–µ—Ä–µ–≥—Ä—ñ—Ç–∞ –ø–∞—Ä–∞). –ü—Ä–∏–º—ñ—Ç–∫–∞: –ü–ª–æ—â—ñ —Ñ—ñ–≥—É—Ä FAB —ñ GCB –æ–¥–Ω–∞–∫–æ–≤—ñ. –ü–µ—Ä–µ–≥—Ä—ñÃÅ—Ç–∞ —Ä—ñ–¥–∏–Ω–∞ÃÅ (–∞–Ω–≥–ª. superheated liquid) ‚Äî —Ä—ñ–¥–∏–Ω–∞, —â–æ –Ω–∞–≥—Ä—ñ—Ç–∞ –¥–æ —Ç–µ–º–ø–µ—Ä–∞—Ç—É—Ä–∏, –≤–∏—â–æ—ó –∑–∞ —Ç–µ–º–ø–µ—Ä–∞—Ç—É—Ä—É –∫–∏–ø—ñ–Ω–Ω—è[1]. –ü–µ—Ä–µ–≥—Ä—ñ—Ç–∞ —Ä—ñ–¥–∏–Ω–∞ —î –ø—Ä–∏–∫–ª–∞–¥–æ–º –º–µ—Ç–∞—Å—Ç–∞–±—ñ–ª—å–Ω–æ–≥–æ —Å—Ç–∞–Ω—É, —è–∫–∏–π –∑–∞ –ø–µ–≤–Ω–∏—Ö —É–º–æ–≤ —É –Ω–∏–∑—Ü—ñ –µ–Ω–µ—Ä–≥–µ—Ç–∏—á–Ω–∏—Ö —ñ —Ç–µ—Ö–Ω–æ–ª–æ–≥—ñ—á–Ω–∏—Ö —Ä–µ–∂–∏–º—ñ–≤ —Å–ø—Ä–∏—á–∏–Ω—è—î —Ç–∞–∫—ñ —Å–ø–µ—Ü–∏—Ñ—ñ—á–Ω—ñ –¥–∏–Ω–∞–º—ñ—á–Ω—ñ —è–≤–∏—â–∞, —è–∫ –≤–∏–±—É—Ö–æ–ø–æ–¥—ñ–±–Ω–µ –∑–∞–∫–∏–ø–∞–Ω–Ω—è –∑–∞ —Ä–∞—Ö—É–Ω–æ–∫ –Ω–∞–∫–æ–ø–∏—á–µ–Ω–æ–≥–æ —Ç–µ–ø–ª–∞, –Ω–µ—Å—Ç—ñ–π–∫—ñ—Å—Ç—å –ø–æ–≤–µ—Ä—Ö–Ω—ñ —Ä–æ–∑–¥—ñ–ª–µ–Ω–Ω—è —Ä—ñ–¥–∏–Ω–∞-–ø–∞—Ä–∞, —Ñ–æ—Ä–º—É–≤–∞–Ω–Ω—è —Ñ—Ä–æ–Ω—Ç—É —Ñ–∞–∑–æ–≤–æ–≥–æ –ø–µ—Ä–µ—Ö–æ–¥—É. –ó–∞–≥–∞–ª—å–Ω—ñ –ø–æ–Ω—è—Ç—Ç—è–í–µ–ª–∏—á–∏–Ω–∞ –ø–µ—Ä–µ–≥—Ä—ñ–≤—É –∑–∞–ª–µ–∂–∏—Ç—å –≤—ñ–¥ –Ω–∏–∑–∫–∏ —Ñ—ñ–∑–∏–∫–æ-—Ö—ñ–º—ñ—á–Ω–∏—Ö –≤–ª–∞—Å—Ç–∏–≤–æ—Å—Ç–µ–π —è–∫ —Å–∞–º–æ—ó —Ä—ñ–¥–∏–Ω–∏, —Ç–∞–∫ —ñ –≥—Ä–∞–Ω–∏—á–Ω–∏—Ö —Ç–≤–µ—Ä–¥–∏—Ö –ø–æ–≤–µ—Ä—Ö–æ–Ω—å. –Ý–µ—Ç–µ–ª—å–Ω–æ –æ—á–∏—â–µ–Ω—ñ —Ä—ñ–¥–∏–Ω–∏ –ø–æ–∑–±–∞–≤–ª–µ–Ω—ñ —Ä–æ–∑—á–∏–Ω–µ–Ω–∏—Ö –≥–∞–∑—ñ–≤ (–ø–æ–≤—ñ—Ç—Ä—è), –º–æ–∂–Ω–∞ –ø—Ä–∏ –¥–æ—Ç—Ä–∏–º–∞–Ω–Ω—ñ –æ—Å–æ–±–ª–∏–≤–∏—Ö –∑–∞–ø–æ–±—ñ–∂–Ω–∏—Ö –∑–∞—Å–æ–±—ñ–≤ –ø–µ—Ä–µ–≥—Ä—ñ—Ç–∏ –Ω–∞ –¥–µ—Å—è—Ç–∫–∏ –≥—Ä–∞–¥—É—Å—ñ–≤ –±–µ–∑ –∑–∞–∫–∏–ø–∞–Ω–Ω—è. –ö–æ–ª–∏ —Ç–∞–∫–∞ –ø–µ—Ä–µ–≥—Ä—ñ—Ç–∞ —Ä—ñ–¥–∏–Ω–∞ –≤—Ä–µ—à—Ç—ñ-—Ä–µ—à—Ç –∑–∞–∫–∏–ø–∞—î, —Ç–æ –ø—Ä–æ—Ü–µ—Å –∫–∏–ø—ñ–Ω–Ω—è –ø—Ä–æ—Ç—ñ–∫–∞—î –≤–µ–ª—å–º–∏ –±—É—Ä—Ö–ª–∏–≤–æ, –Ω–∞–≥–∞–¥—É—é—á–∏ –≤–∏–±—É—Ö. –ó–∞–∫–∏–ø–∞–Ω–Ω—è –ø–µ—Ä–µ–≥—Ä—ñ—Ç–æ—ó —Ä—ñ–¥–∏–Ω–∏ —Å—É–ø—Ä–æ–≤–æ–¥–∂—É—î—Ç—å—Å—è —Ä–æ–∑–±—Ä–∏–∑–∫—É–≤–∞–Ω–Ω—è–º —Ä—ñ–¥–∏–Ω–∏, –≥—ñ–¥—Ä–∞–≤–ª—ñ—á–Ω–∏–º–∏ —É–¥–∞—Ä–∞–º–∏ –π —ñ–Ω–∫–æ–ª–∏ –Ω–∞–≤—ñ—Ç—å —Ä—É–π–Ω—É–≤–∞–Ω–Ω—è–º –ø–æ—Å—É–¥–∏–Ω–∏. –¢–µ–ø–ª–æ—Ç–∞ –ø–µ—Ä–µ–≥—Ä—ñ–≤—É –≤–∏—Ç—Ä–∞—á–∞—î—Ç—å—Å—è –Ω–∞ –ø–∞—Ä–æ—Ç–≤–æ—Ä–µ–Ω–Ω—è, —Ç–æ–º—É —Ä—ñ–¥–∏–Ω–∞ —à–≤–∏–¥–∫–æ –æ—Ö–æ–ª–æ–¥–∂—É—î—Ç—å—Å—è –¥–æ —Ç–µ–º–ø–µ—Ä–∞—Ç—É—Ä–∏ –Ω–∞—Å–∏—á–µ–Ω–æ—ó –ø–∞—Ä–∏, –∑ —è–∫–æ—é –≤–æ–Ω–∞ –ø–µ—Ä–µ–±—É–≤–∞—î —É —Ä—ñ–≤–Ω–æ–≤–∞–∑—ñ. –ú–æ–∂–ª–∏–≤—ñ—Å—Ç—å –∑–Ω–∞—á–Ω–æ–≥–æ –ø–µ—Ä–µ–≥—Ä—ñ–≤–∞–Ω–Ω—è —á–∏—Å—Ç–æ—ó —Ä—ñ–¥–∏–Ω–∏ –±–µ–∑ –∫–∏–ø—ñ–Ω–Ω—è –ø–æ—è—Å–Ω—é—î—Ç—å—Å—è —É—Ç—Ä—É–¥–Ω–µ–Ω—ñ—Å—Ç—é –≤–∏–Ω–∏–∫–Ω–µ–Ω–Ω—è –ø–æ—á–∞—Ç–∫–æ–≤–∏—Ö –º–∞–ª–µ–Ω—å–∫–∏—Ö –±—É–ª—å–±–∞—à–æ–∫ (–∑–∞—Ä–æ–¥–∫—ñ–≤), —ó—Ö —É—Ç–≤–æ—Ä–µ–Ω–Ω—é –ø–µ—Ä–µ—à–∫–æ–¥–∂–∞—î –∑–Ω–∞—á–Ω–µ –≤–∑–∞—î–º–Ω–µ –ø—Ä–∏—Ç—è–≥–∞–Ω–Ω—è –º–æ–ª–µ–∫—É–ª —Ä—ñ–¥–∏–Ω–∏. –ü–æ —ñ–Ω—à–æ–º—É –≤—ñ–¥–±—É–≤–∞—î—Ç—å—Å—è, –∫–æ–ª–∏ —Ä—ñ–¥–∏–Ω–∞ –º—ñ—Å—Ç–∏—Ç—å —Ä–æ–∑—á–∏–Ω–µ–Ω—ñ –≥–∞–∑–∏ –π —Ä—ñ–∑–Ω—ñ –Ω–∞–π–¥—Ä—ñ–±–Ω—ñ—à—ñ –∑–∞–≤—ñ—à–µ–Ω—ñ —Ç–≤–µ—Ä–¥—ñ —á–∞—Å—Ç–æ—á–∫–∏. –í —Ü—å–æ–º—É –≤–∏–ø–∞–¥–∫—É –≤–∂–µ –Ω–µ–∑–Ω–∞—á–Ω–µ –ø–µ—Ä–µ–≥—Ä—ñ–≤–∞–Ω–Ω—è (–Ω–∞ –¥–µ—Å—è—Ç—ñ –¥–æ–ª—ñ –≥—Ä–∞–¥—É—Å–∞) –≤–∏–∫–ª–∏–∫–∞—î —Å—Ç—ñ–π–∫–µ —ñ —Å–ø–æ–∫—ñ–π–Ω–µ –∫–∏–ø—ñ–Ω–Ω—è, –æ—Å–∫—ñ–ª—å–∫–∏ –ø–æ—á–∞—Ç–∫–æ–≤–∏–º–∏ –∑–∞—Ä–æ–¥–∫–∞–º–∏ –ø–∞—Ä–æ–≤–æ—ó —Ñ–∞–∑–∏ —Å–ª—É–∂–∞—Ç—å –≥–∞–∑–æ–≤—ñ –±—É–ª—å–±–∞—à–∫–∏ —Ç–∞ —Ç–≤–µ—Ä–¥—ñ —á–∞—Å—Ç–∫–∏. –û—Å–Ω–æ–≤–Ω—ñ —Ü–µ–Ω—Ç—Ä–∏ –ø–∞—Ä–æ—É—Ç–≤–æ—Ä–µ–Ω–Ω—è –º–∞—é—Ç—å –º—ñ—Å—Ü–µ –≤ —Ç–æ—á–∫–∞—Ö –ø–æ–≤–µ—Ä—Ö–Ω—ñ, –¥–æ —è–∫–æ—ó –ø—ñ–¥–≤–æ–¥–∏—Ç—å—Å—è —Ç–µ–ø–ª–æ —ñ —î –Ω–∞–π–¥—Ä—ñ–±–Ω—ñ—à—ñ –ø–æ—Ä–∏ –∑ –∞–¥—Å–æ—Ä–±–æ–≤–∞–Ω–∏–º –≥–∞–∑–æ–º, –∞ —Ç–∞–∫–æ–∂ —Ä—ñ–∑–Ω—ñ –Ω–µ–æ–¥–Ω–æ—Ä—ñ–¥–Ω–æ—Å—Ç—ñ, –≤–∫–ª—é—á–µ–Ω–Ω—è —ñ –Ω–∞–ª—å–æ—Ç–∏, —è–∫—ñ –∑–Ω–∏–∂—É—é—Ç—å –º–æ–ª–µ–∫—É–ª—è—Ä–Ω–µ –∑—á–µ–ø–ª–µ–Ω–Ω—è —Ä—ñ–¥–∏–Ω–∏ –∑ –ø–æ–≤–µ—Ä—Ö–Ω–µ—é. –£–º–æ–≤–∏ —ñ—Å–Ω—É–≤–∞–Ω–Ω—è –ø–µ—Ä–µ–≥—Ä—ñ—Ç–æ—ó —Ä—ñ–¥–∏–Ω–∏–Ü—Å–Ω—É–≤–∞–Ω–Ω—è –ø–µ—Ä–µ–≥—Ä—ñ—Ç–∏—Ö (–º–µ—Ç–∞—Å—Ç–∞–±—ñ–ª—å–Ω–∏—Ö) —Å—Ç–∞–Ω—ñ–≤ –ø–æ–≤'—è–∑–∞–Ω–µ —ñ–∑ —É—Ç—Ä—É–¥–Ω–µ–Ω—ñ—Å—Ç—é –ø–æ—á–∞—Ç–∫–æ–≤–æ—ó —Å—Ç–∞–¥—ñ—ó —Ñ–∞–∑–æ–≤–æ–≥–æ –ø–µ—Ä–µ—Ö–æ–¥—É –ø–µ—Ä—à–æ–≥–æ —Ä–æ–¥—É. –ü—Ä–µ—Ä–∏–≤—á–∞—Å—Ç–∏–π —Ö–∞—Ä–∞–∫—Ç–µ—Ä –ø–µ—Ä–µ—Ö–æ–¥—É (, ; —Ç—É—Ç ‚Äî –ø–∏—Ç–æ–º–∞ –µ–Ω—Ç—Ä–æ–ø—ñ—è, ‚Äî –ø–∏—Ç–æ–º–∏–π –æ–±'—î–º) –≤–∏–∫–ª—é—á–∞—î –º–æ–∂–ª–∏–≤—ñ—Å—Ç—å –ø–µ—Ä–µ—Ç–≤–æ—Ä–µ–Ω–Ω—è –æ–¥–Ω–æ—á–∞—Å–Ω–æ —É –≤—Å—ñ–π –º–∞—Å—ñ —Ä–µ—á–æ–≤–∏–Ω–∏ —É —Å—Ç–∞–Ω—ñ, –±–ª–∏–∑—å–∫–æ–º—É –¥–æ —Ñ–∞–∑–æ–≤–æ—ó —Ä—ñ–≤–Ω–æ–≤–∞–≥–∏. –§–∞–∑–æ–≤–∏–π –ø–µ—Ä–µ—Ö—ñ–¥ –ø–æ—á–∏–Ω–∞—î—Ç—å—Å—è –≤ –æ–∫—Ä–µ–º–∏—Ö ¬´—Ç–æ—á–∫–∞—Ö¬ª –æ–¥–Ω–æ—Ä—ñ–¥–Ω–æ—ó —Å–∏—Å—Ç–µ–º–∏, —Ü—ñ —Ç–æ—á–∫–∏ –ø–æ–≤–∏–Ω–Ω—ñ –∑–∞–¥–æ–≤–æ–ª—å–Ω—è—Ç–∏ —É–º–æ–≤—É ( ‚Äî —Ä–∞–¥—ñ—É—Å –∑–∞—Ä–æ–¥–∫–∞, ‚Äî —Ä–∞–¥—ñ—É—Å –∫—Ä–∏—Ç–∏—á–Ω–æ–≥–æ –∑–∞—Ä–æ–¥–∫–∞) ‚Äî —Ç–æ–¥—ñ —Ä—ñ—Å—Ç –Ω–æ–≤–æ—ó —Ñ–∞–∑–∏ —Å—É–ø—Ä–æ–≤–æ–¥–∂—É—î—Ç—å—Å—è –∑–º–µ–Ω—à–µ–Ω–Ω—è–º —Ç–µ—Ä–º–æ–¥–∏–Ω–∞–º—ñ—á–Ω–æ–≥–æ –ø–æ—Ç–µ–Ω—Ü—ñ–∞–ª—É. –•–∞—Ä–∞–∫—Ç–µ—Ä–∏—Å—Ç–∏–∫–æ—é –ø–æ—Ç–µ–Ω—Ü—ñ–∞–ª—å–Ω–æ–≥–æ –±–∞—Ä'—î—Ä—É, —è–∫–∏–π —Å–ª—ñ–¥ –ø–æ–¥–æ–ª–∞—Ç–∏ –∑–∞—Ä–æ–¥–∫—É –¥–ª—è –¥–æ—Å—è–≥–Ω–µ–Ω–Ω—è –∫—Ä–∏—Ç–∏—á–Ω–æ–≥–æ —Ä–æ–∑–º—ñ—Ä—É, —î —Ä–æ–±–æ—Ç–∞ –∑ —É—Ç–≤–æ—Ä–µ–Ω–Ω—è –∫—Ä–∏—Ç–∏—á–Ω–æ–≥–æ –∑–∞—Ä–æ–¥–∫–∞: –¥–µ
також можна записати через рівноважні властивості: де — коефіцієнт поверхневого натягу. ПрикладиЯкщо з рідини видалити розчинене повітря (багатократним кип'ятінням) і можливі центри пароутворення (пилинки, іони тощо), то можна нагріти рідину до температури, дещо вищої від температури кипіння. Такий стан називається перегрітою рідиною. Стан перегрітої рідини також можна одержати і при зниженні зовнішнього тиску до рівня нижчого за тиск насиченої пари рідини за даної температури. Аргон за атмосферного тиску:
Звідси видно, що досяжне перегрівання становить 44 градуси. Вода дозволяє стійке перегрівання до 200 °C. Нагріта до 300 °C вода може існувати у рідкому стані за атмосферного тиску протягом часу порядку декількох мікросекунд. Див. такожПримітки
–î–∂–µ—Ä–µ–ª–∞
–ü–æ—Å–∏–ª–∞–Ω–Ω—è
|
Portal di Ensiklopedia Dunia
































