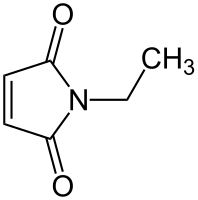
N-Этилмалеимид
N-Этилмалеимид (НЭМ) — производное малеиновой кислоты. Он содержит имидную функциональную группу и представляет собой активированный алкен, который реагирует с тиолами и часто используется для модификации остатков цистеина в белках и пептидах[1]. Химические свойстваN-Этилмалеимид является акцептором Михаэля. Это означает, что он может присоединять нуклеофилы, такие как тиолы. Образовавшийся в результате такой реакции тиоэфир обладает очень прочной C–S-связью, и реакция является практически необратимой. Реакция протекает при рН 6,5—7,5. N-этилмалеимид может реагировать с аминами или подвергаться гидролизу при более щелочных рН. N-этилмалеимид широко использовался для определения функциональной роли тиольных групп в энзимологии. Он является необратимым ингибитором всех цистеиновых пептидаз, поскольку осуществляет алкилирование тиольных групп в активном центре (см. схему)[2][3].  Тематические исследованияНЭМ блокирует везикулярный транспорт. Лизисные буферы с 20—25 мМ N-этилмалеимида используются для ингибирования де-сумоилирования белков во время вестерн-блоттинга. НЭМ также используется в качестве ингибитора деубиквитинилирования. Артур Корнберг и его коллеги использовали N-этилмалеимид, чтобы выключить ДНК-полимеразу III и сравнить её активность с ДНК-полимеразой I. Корнберг был удостоен Нобелевской премии за открытие ДНК-полимеразы I, которая в то время считалась главной полимеразой бактериальной репликации, хотя позже его сын Томас показал, что основной репликативной полимеразой у бактерий является ещё не открытая в то время ДНК-полимераза III. N-Этилмалеимид активирует оуабаин-нечувствительное хлор-зависимое поступление ионов калия в красные кровяные тельца овец и коз[4]. Шестнадцать лет спустя это открытие способствовало открытию K+/Cl- котранспортёров в клетках человеческих эмбрионов, в которые ввели кДНК изоформы по KCC1[5]. С тех пор N-этилмалеимид широко используется в качестве диагностического инструмента для определения наличия K+/Cl- симпортов в клетках разных видов животных[6][7][8][9]. Примечания
Внешние ссылки
|
||||||||||||||||||||||||||||||||||||||||||||||
Portal di Ensiklopedia Dunia