žóľŪôĒ Ž≤†Ž¶īŽ•®
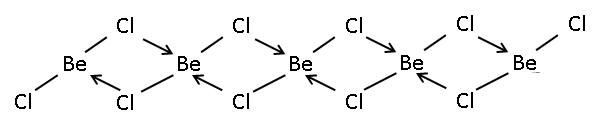
žóľŪôĒ Ž≤†Ž¶īŽ•®(Beryllium chloride)žĚÄ BeCl2žĚė ŪôĒŪēôžč̞̥ ÍįÄžßÄŽäĒ Ž¨īÍłį ŪôĒŪē©Ž¨ľŽ°ú, žóľžÜĆžôÄ Ž≤†Ž¶īŽ•®žĚī Í≤įŪē©Ūēú Ž¨ľžßąžĚīŽč§. žÉĀžė®žóźžĄú Ž¨īžÉČžĚė ŪĚ°žäĶžĄĪ Í≥†ž≤īŽ°ú Í∑ĻžĄĪ žö©Žß§žóź žěė žö©ŪēīŽźúŽč§. Ž≤†Ž¶īŽ•®žĚė žõźžěź ŽįėžßÄŽ¶ĄÍ≥ľ ž†ĄŪēėŽüČžĚė ŽĻĄžú®žĚī žēĆŽ£®ŽĮłŽäĄžĚė Í∑łÍ≤ÉÍ≥ľ ŽĻĄžä∑ŪēėŽĮÄŽ°ú žóľŪôĒ žēĆŽ£®ŽĮłŽäĄ(AlCl3)Í≥ľŽŹĄ žĄĪžßąžĚī ŽĻĄžä∑ŪēėŽč§. ÍĶ¨ž°įÍ≥†ž≤ī žÉĀŪÉúžĚė žóľŪôĒ Ž≤†Ž¶īŽ•®žĚÄ 1žį®žõźžĚė ž§ĎŪē©ž≤īŽ°ú ž°īžě¨ŪēúŽč§. žĚīŽ•ľ ÍįÄžóīŪēėžó¨ Íłįž≤īŽ°ú ŽßƎ硫©ī žĄ†ŪėēžĚė Žč®žúĄž≤īŽāė ŽĎź ÍįúžĚė žóľžÜĆ žõźžěźŽ°ú žóįÍ≤įŽźú žĚīŪē©ž≤īŽ°ú Ž∂ĄŪēīŽźúŽč§. žĚīŪē©ž≤īžĚľ ŽēĆ Ž≤†Ž¶īŽ•®žĚė ŽįįžúĄžąėŽäĒ 3žĚīŽč§. Žč§Ž•ł 2ÍįÄ ÍłąžÜć žĖĎžĚīžė®žĚė Ūē†Ž°úž††ŪôĒŽ¨ľÍ≥ľŽäĒ Žč¨Ž¶¨ VSEPR žĚīŽ°†žóź ŽĒįŽĚľ žĄ†ŪėēžĚė ÍĶ¨ž°įŽ•ľ ÍįĞߥŽč§. ž†úŽ≤ē ŽįŹ ŽįėžĚĎžóľŪôĒ Ž≤†Ž¶īŽ•®žĚÄ Ž≤†Ž¶īŽ•®žĚĄ žóľžÜĆ Ž∂ĄžěźžôÄ Í≥†žė®žóźžĄú žßĀž†Ď ŽįėžĚĎžčúŪā§ÍĪįŽāė žąúžąėŪēú Ž≤†Ž¶īŽ•® ÍłąžÜćžĚīŽāė žāįŪôĒ Ž≤†Ž¶īŽ•®, žąėžāįŪôĒ Ž≤†Ž¶īŽ•®žĚĄ žóľžāįÍ≥ľ ŽįėžĚĎžčúžľú žĖĽŽäĒŽč§. žóľžÜĆžĚė ž°īžě¨ Ūēėžóź žāįŪôĒ Ž≤†Ž¶īŽ•®žĚĄ ŪÉĄžÜĆžôÄ ŽįėžĚĎžčúžľú žĖĽÍłįŽŹĄ ŪēúŽč§. žóľŪôĒ Ž≤†Ž¶īŽ•®žĚÄ ÍĪīž°įŪēú Í≥ĶÍłįžóźžĄúŽäĒ žēąž†ēŪēėžßÄŽßĆ ŪĚ°žäĶžĄĪžĚī ŪĀ¨Í≥†, Ž¨ľžóź žö©ŪēīŽź† ŽēĆ žóīžĚī ŽįúžÉĚŪēėŽ©īžĄú 4žąėŪôĒŽ¨ľ(BeCl2¬∑4H2O)žĚī žÉĚžĄĪŽźúŽč§. Ž£®žĚīžä§ žāįžĚīŽ©į, ŪĒĄŽ¶¨Žćł-ŪĀ¨ŽěėŪĒĄžł† ŽįėžĚĎÍ≥ľ ÍįôžĚÄ žĚľŽ∂Ä žú†Íłį ŪôĒŪēô ŽįėžĚϞ󟞥úŽäĒ žīȎߧŽ°ú žěĎžö©ŪēúŽč§. žóźŪĄįžôÄ ÍįôžĚī žāįžÜĆŽ•ľ ŪŹ¨Ūē®ŪēėŽäĒ žö©Žß§žóź žěė žö©ŪēīŽźúŽč§. žąúžąėŪēú Ž≤†Ž¶īŽ•®žĚĄ žÉĚžāįŪē† ŽēĆ žóľŪôĒ Ž≤†Ž¶īŽ•®žĚĄ žóľŪôĒ ŽāėŪ䳎•®Í≥ľ Ūē®ÍĽė žö©žúĶžčúžľú ž†ĄÍłįŽ∂ĄŪēīŪēėžó¨ žĖĽŽäĒŽč§.
ÍįôžĚī Ž≥īÍłįÍįĀž£ľ
žôłŽ∂Ä ŽßĀŪĀ¨
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Portal di Ensiklopedia Dunia