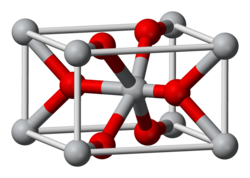
‰∫åÊ∞ßÂåñÈä• ÂåñÂ≠∏ºè ÁÇ∫IrO2 ÔºåÊòØÂî؉∏ÄÊòéÁ¢∫Áü•ÈÅìÂÖ∂ÁâπÊÄßÁöÑÈä•Ê∞ßÂåñÁâ©ÔºåÂÖ∂Êô∂Êݺ ÁÇ∫ÈáëÁ∫¢Áü≥ TiO2 ÁµêÊßãÔºåÂÖ∂‰∏≠ÊúâÂÖ≠ÈÖç‰ΩçÁöÑÈä• Âèä‰∏âÈÖç‰ΩçÁöÑÊ∞ß [ 1]
‰∫åÊ∞ßÂåñÈä•ÂíåÂÖ∂‰ªñÁ®ÄÊúâÈá뱨 ÁöÑÊ∞ßÂåñÁâ©ÂèØÁî®Âú®Â∑•Ê•≠ÈõªËߣ ÁöÑÈôΩÊ•µÈõªÊ•µ Ժ剪•ÂèäÁîµÁîüÁêÜÂ≠¶ ÁÝîÁ©∂‰∏≠Áî®Âà∞ÁöÑÂæÆÈõªÊ•µ [ 2]
二氧化銥可以由銥黑(細粉末狀的銥金屬)在空气或氧中氧化 來製備:
I
r
+
O
2
‚Üí
700
o
C
I
r
O
2
.
{\displaystyle \mathrm {Ir+O_{2}\ {\xrightarrow {700^{o}C}}\ IrO_{2}} .}
ÂùóÁä∂Èáë±ûÈì±Âú®Á©∫Ê∞î‰∏≠ÂäÝÁÉ≠Êó∂‰ºöÂΩ¢Êàê‰∫åÊ∞ßÂåñÈì±ËñÑËÜú„ÄÇ
Ê≤∏ËÖæÁöÑÂÖ≠Ê∞ØÂêàÈì±(IV)ÈÖ∏ÁõêÂíåÁ¢±ÂèçÂ∫îÂπ∂Âú®ÁúüÁ©∫ ‰∏≠Âπ≤Áá•ÔºåÂè؉ª•ÂæóÂà∞IrO2 ¬∑2H2 OÔºåÂÜçÂ∞ÜÂÖ∂Âú®Ê∞ÆÊ∞î ‰∏≠ÂäÝÁÉ≠Ëá≥350‚ÑÉÔºåÂæóÂà∞ȪëËâ≤ÁöÑIrO2 „ÄÇ
I
r
O
2
‚ãÖ
2
H
2
O
‚Üí
300
o
C
I
r
O
2
+
2
H
2
O
.
{\displaystyle \mathrm {IrO_{2}\cdot 2H_{2}O\ {\xrightarrow {300^{o}C}}\ IrO_{2}+2H_{2}O} .}
二氧化铱中,铱显+4价,对热稳定,是最稳定的铱氧化物,在1100℃下不会分解[ 3] 硝酸 、硫酸 或者碱 ,但可以和盐酸 或氢溴酸 反应,分别生成[IrCl6 ]2- 和[IrBr6 ]2- 配离子。[ 4]
二氧化铱可以用于制作涂层电极 。[ 5]
^ Greenwood, N. N.; Earnshaw, A. Chemistry of the Elements ISBN 0-7506-3365-4 ^ Cogan, Stuart F. Neural Stimulation and Recording Electrodes. Annual Review of Biomedical Engineering. August 2008, 10 (1): 275‚Äì309. doi:10.1146/annurev.bioeng.10.061807.160518 ^ Ë∞¢È´òÈò≥, Áî≥Ê≥ÆÊñá, ÂæêÁªçÁé≤ Á≠â. „ÄäÊóÝÊú∫ÂåñÂ≠¶‰∏õ‰π¶„ÄãÁ¨¨‰πùÂç∑ Èî∞ÂàÜÊóè ÈìÅÁ≥ª ÈìÇÁ≥ª. ÁßëÂ≠¶Âá∫ÁâàÁ§æ,2011. pp 405. 5.2 Èì±Áöщ∫åÂÖÉÂåñÂêàÁâ©. Ë°®5.5 Âç§ÂåñÁâ©ÂèäÁ°´ÊóèÂåñÂêàÁâ©. ISBN 978-7-03-030545-9
^ Êú±ÊñáÁ••. ÊóÝÊú∫ÂåñÂêàÁâ©Âà∂§áÊâãÂÜå[M]. ÂåñÂ≠¶Â∑•‰∏öÂá∫ÁâàÁ§æ. 2006.9. pp 349. „Äê‚Ö®-44„Äë ‰∫åÊ∞ßÂåñÈì± [iridium(IV) oxide]. ISBN 7-5025-8537-0
^ ÂêëÂâç, ȪÑÊ∞∏Êòå, Âç¢Ê¥™ Á≠â. ÊîπÊÄ߉∫åÊ∞ßÂåñÈì±ÁîµÊûÅÁÝîÂà∂[J]. ÊóÝÊú∫ÁõêÂ∑•‰∏ö. 1998, 30(3): 16~17, 42
Èì±(0) Èì±(I) Èì±(II) Èì±(III) Èì±(IV) Èì±(V) Èì±(VI) Èì±(VII) Èì±(VIII) Èì±(IX)