최초로 분리된 단일 알칼로이드인 모르핀 은 1804년 양귀비 (Papaver somniferum )로부터 분리되었다.[ 1] 알칼로이드 (alkaloid, 유염기, 식물염기)는 자연적으로 존재하면서 대개 염기 로 질소 원자를 가지는 화합물 의 총칭이다. 대부분의 물질은 염기성이지만 일부 중성이나[ 2] [ 3] [ 4] 탄소 와 수소 , 질소 는 기본이며 알칼로이드 분자는 또한 황 과 드물게 염소 , 브로민 , 인 까지 포함할 수도 있다.[ 5]
알칼로이드는 천연물 이나 이차대사산물 의 일종으로, 박테리아 나 균류 , 식물 , 동물 을 비롯한 다양한 생물군에서 얻을 수 있다. 많은 알칼로이드는 천연 그대로 뽑아낸 것을 산염기 추출 을 통해 정제가 가능하다. 다른 생체 에 대해 독성 을 띠는 것이 많다. 흔히 약리학 적 효과를 가지므로 의약품 이나 마약 등으로, 신내림 의식 등에서도 사용된다. 대표적인 알칼로이드로 국소 마취제이자 흥분제 인 코카인 , 흥분제 카페인 과 니코틴 , 진통제 모르핀 , 말라리아약으로 쓰는 퀴닌 등이 있다. 서로 다른 알칼로이드는 사람과 동물 물질대사 의 서로 다른 부분에 작용하나 맛은 한결같이 쓰다.[ 6]
알칼로이드와 다른 함질소 자연 화합물의 경계는 그리 명확하지 않다.[ 7] 아미노산 펩타이드 , 단백질 , 뉴클레오타이드 , 핵산 , 아민 같은 종류의 분자는 대개 알칼로이드라 부르지 않는다.[ 2] 메스칼린 , 세로토닌 , 도파민 , 등)도 대개 알칼로이드가 아니라 아민 의 일종이라 보는데,[ 8] [ 9] [ 10] [ 11]
"알칼로이드"라는 개념을 처음 도입한 논문. "알칼로이드"라는 이름은 1819년 독일의 약제사 Carl F.W. Meissner가 처음 사용한 것으로, 라틴어 어근 alkali 알칼리[* ] ("식물의 재"를 뜻하는 al qualja 알 쿠알자[* ] 에서 옴)와 그리스어 접미사 ειδοσ 에이도스[* ] 에서 파생되었다. 이 말은 사용되지 않다가 1880년대 O. Jacobsen이 Albert Ladenburg 화학용어사전에서 재발견한 후에야 널리 사용되기 시작했다.[ 12]
개개의 알칼로이드를 명명하는 단일한 규정은 없다.[ 13] 벨라돈나풀 에서 추출하는 아트로핀 은 그 속명 아트로파에서, 마전 의 씨에서 얻는 스트리키니네 는 역시 그 속명 스트리크노스(마전속)에서 이름을 따온 것이다.[ 5] 빙카속 (Vinca ) 식물에서 뽑아낸 알칼로이드로서 어근 "vin"을 가진 알칼로이드는 86종이나 된다.[ 14]
알칼로이드를 포함한 식물은 고대부터 치료용이나 기분 전환용으로 사용되었다. 메소포타미아 에서는 기원전 2000년 즈음부터 약용으로 쓰는 식물이 알려져 있었다.[ 15] 호메로스 의 《오디세이아 》에는 이집트 여왕이 헬렌에게 주었다는 선물, 즉 망각을 부르는 약이 나온다. 그 선물이란 것은 아편이 포함된 약으로 생각된다.[ 16] 마황 과 양귀비 의 의학적 효능에 대해 언급한다.[ 17] 코카나무 잎 역시 오래전부터 남아메리카 인디언이 사용해왔다.[ 18]
아코니틴 , 튜보크라린 같이 독성 알칼로이드를 함유한 식물에서 뽑아낸 추출물은 고대부터 독화살의 화살축에 바르는데 쓰였다.
알칼로이드 연구는 19세기에 시작되었다. 1804년에 독일 화학자 프리드리히 제르튀르너 (Friedrich Sertürner)는 아편초로부터 "잠의 근원"(라틴어 : principium somniferum )을 분리해내어서, 그리스 신화의 꿈의 신 모르페우스 에 대한 경의로 "모르피움"이라는 이름을 붙였다. 이 약이 지금의 모르핀 이다.
프랑스의 연구자 피에르 조제프 펠티에 와 조제프 비앵네메 카방투 는 퀴닌 (1820)과 스트리키니네 (1818)을 발견하면서 성장 초기 알칼로이드 화학에서 소중한 성과를 얻어냈다. 이후 크산틴 (1817), 아트로핀 (1819), 카페인 (1820), 코닌 (1827), 니코틴 (1828), 콜히친 (1833), 스파르테인 (1851), 코카인 (1860) 등 다른 알칼로이드가 속속 발견되었다.[ 19]
1886년에는 독일 화학자 라덴부르크(Albert Ladenburg)가 알칼로이드의 하나인 코닌 을 인공적으로 합성하는 데 성공했다. 2-메틸피리딘을 아세트알데히드 와 반응시키고 거기서 나온 2-프로페닐피리딘을 나트륨 으로 분해함으로써 코닌을 얻었다.[ 20] [ 21] 분광학 과 크로마토그래피 의 출현으로 알칼로이드 화학은 한층 가속되었고, 2008년까지 12,000개 이상의 알칼로이드가 식별되었다.
두꺼비 독 부포테닌 (Bufotenin). 인돌 핵이 있으며 아미노산 트립토판 으로부터 살아있는 생물에서 합성된다. 알칼로이드는 대부분의 다른 자연 화합물에 비해 구조가 꽤나 다양하다는 것이 특성이며 알칼로이드를 분류하는 일관된 방법은 없다.[ 22] [ 5] [ 23]
현대의 다른 분류들은 탄소 뼈대의 유사성이나(인돌 알칼로이드, 이소퀴놀린 알칼로이드, 피리딘 알칼로이드 따위), 생물 발생상의 전구체(오르니틴계, 리신계, 타이로신계, 트립토판계 등)에 근거한다.[ 5] [ 22] 니코틴 은 니코틴아마이드 에서 만들어진 피리딘 조각과 오르니틴에서 만들어진 피롤리딘 부분을 포함하고 있고[ 24] [ 25]
알칼로이드는 대개 다음의 주분류군으로 나뉜다:[ 26]
"진정알칼로이드(True alkaloids)" - 이종고리 에 질소 를 가지며 아미노산 에서 비롯된 것.[ 27] 아트로핀 , 니코틴 , 모르핀 등이다. 또한 피페르딘 알칼로이드인 코민 이나 코니세인 은[ 28] [ 29]
"원시알칼로이드(Protoalkaloids)" - 질소를 가지며 역시 아미노산에서 비롯된 것.[ 27] 메스칼린 , 아드레날린 , 에페드린 등이 있다.
폴리아민 알칼로이드 - 푸트레신 계, 스페르미딘 계, 스페르민 계 따위
펩타이드 및 사이클로펩타이드 알칼로이드[ 30]
유사알칼로이드(Pseudalkaloids) - 아미노산에서 비롯되지 않았으나 알칼로이드와 유사한 화합물.[ 31] 테르펜 알칼로이드, 스테로이드 알칼로이드를 비롯하여,[ 32] 카페인 이나 테오브로민 , 테오필린 등이 속한 푸린 알칼로이드가 있다.[ 33] 에페드린 이나 카티논 을 유사알칼로이드로 분류하는데, 이것들은 아미노산인 페닐알라닌 에서 비롯되긴 하지만 그 질소 원자를 아미노산이 아니라 아미노기 전이 과정에서 얻는다.[ 33] [ 34] 어떤 알칼로이드의 경우 해당 주분류군의 특징이 되는 탄소 골격이 없다. 그래서 갈란타민 이나 호모아포르핀 같은 것은 이소퀴놀린 조각을 포함하지 않음에도 일반적으로 이소퀴놀린알칼로이드에 넣는다.[ 35]
아래 표는 단합체 알칼로이드의 주요 종류를 나열한 것이다.
계통
분류군
주된 합성 과정
예
질소 이종고리가 있는 알칼로이드 (진정알칼로이드)
필로리딘 계[ 36]
오르니틴 또는 아르기닌 → 푸트레신 → N-메틸푸트레신 → N-메틸-Δ1 -피롤린[ 37] 히그린(Hygrine), hygroline, 스타키드린(stachydrine)[ 36] [ 38]
트로판 계[ 39] 아트로핀 군Substitution in positions 3, 6 or 7
오르니틴 또는 아르기닌 → 푸트레신 → N-메틸푸트레신 → N-메틸-Δ1 -피롤린[ 37] 아트로핀 , 스코폴라민 , 히오시아민 [ 36] [ 39] [ 40]
코카인 군Substitution in positions 2 and 3
코카인 , 엑고닌 (ecgonine)[ 39] [ 41]
피롤리지딘 계[ 42] 비에스테르(Non-esters)
식물에서: 오르니틴 또는 아르기닌 → 푸트레신 → 호모스페르미딘(homospermidine) → retronecine [ 37]
Retronecine , heliotridine, laburnine[ 42] [ 43]
모노카르복실산 복합 에스테르
Indicine, lindelophin, 사라신(sarracine)[ 42]
거대환고리(Macrocyclic) 다이에스테르
플래티필린 (Platyphylline), trichodesmine[ 42]
1-아미노필로리지딘 (lolines )
균류 에서: L -프롤린L -호모세린N -(3-아미노-3-카르복시프로필)프롤린 → norloline[ 44] [ 45] 로린(Loline), N -formylloline, N -acetylloline[ 46]
피페리딘 계[ 47]
리신 → 카다베린 → Δ1 -피페리딘[ 48] Sedamine , lobeline, anaferine, 피페린 (piperine)[ 28] [ 49]
옥탄산 → 코니신 → 코닌 [ 29] 코닌, 코니신[ 29]
퀴놀리지딘 계[ 50] [ 51] 루피닌 군
리신(Lysine) → 카다베린 (cadaverine) → Δ1 -피페리딘(piperideine)[ 52]
루피닌 (lupinine), nupharidin[ 50]
시티신 군
시티신(Cytisine)[ 50]
스파르테인 군
스파르테인 (Sparteine), 루파닌 (lupanine), anahygrine [ 50]
마트린 군
마트린, 옥시마트린(oxymatrine), 알로마트린(allomatridine)[ 50] [ 53] [ 54]
Ormosanine 군
Ormosanine, piptantine[ 50] [ 55]
인돌리지딘 계[ 56]
리신 → α-아미노아디핀산 의 δ-세미알데히드 → 피페콜산 → 1 인돌리지딘[ 57]
스와인소닌 (Swainsonine), 카스타노스페르민 (castanospermine)[ 58]
피리딘 계[ 59] [ 60] 단순 피리딘계 물질
니코틴산 → 다이하이드로니코틴산(dihydronicotinic acid) → 1,2-다이하이드로피리딘(dihydropyridine)[ 61] 트리고넬린 , 리시닌 , 아레콜린 [ 59] [ 62]
다환비응축피리딘계(Polycyclic noncondensing-)
니코틴 , 노르니코틴, 아나바신 , 아나타빈(anatabine)[ 59] [ 62]
다환응축피리딘계(Polycyclic condensed-)
액티니딘 (Actinidine), 겐치아닌(gentianine), pediculinine[ 63]
세스퀴테르펜 -피리딘계
니코틴산 , 이소류신 (isoleucine)[ 11] 에보닌(Evonine), hippocrateine, triptonine[ 60] [ 61]
이소퀴놀린 계 및 관련 알칼로이드[ 64] 단순 이소퀴놀린계 물질[ 65]
티로신 (Tyrosine) 또는 페닐알라닌 (phenylalanine) → 도파민 (dopamine) 또는 티라민 (tyramine) (for alkaloids Amarillis)[ 66] [ 67] 살솔린(Salsoline), lophocerine[ 64] [ 65]
1- 및 3-이소퀴놀린계 물질[ 68]
N-methylcoridaldine, noroxyhydrastinine[ 68]
1- 및 4-페닐테트라하이드로이소퀴놀린계 물질[ 65]
Cryptostilin[ 65] [ 69]
5-나프틸-이소퀴놀린계 물질[ 70]
Ancistrocladine[ 70]
1- 및 2-벤질-이소퀴놀린계 물질[ 71]
파파베린 (Papaverine), 라우다노신 (laudanosine), sendaverine
Cularine group[ 72] Cularine, yagonine[ 72]
Pavines and isopavines[ 73] Argemonine, amurensin [ 73]
Benzopyrrocolines[ 74]
Cryptaustoline[ 65]
Protoberberines[ 65]
베르베린 , 카나딘 , ophiocarpine, mecambridine, corydaline[ 75]
Phtalidisoquinolines[ 65]
히드라스틴 , 나르코틴 , 노스카핀 [ 76]
Spirobenzylisoquinolines[ 65]
Fumaricine[ 73]
토근 알칼로이드[ 77] 에메틴 (Emetine), 프로토에메틴(protoemetine), ipecoside[ 77]
Benzophenanthridines[ 65]
산구이나린(Sanguinarine), oxynitidine, 코리놀록신(corynoloxine)[ 78]
Aporphines [ 65] 글라우신 , 코리딘(coridine), 리리오데닌(liriodenine)[ 79]
Proaporphines[ 65]
Pronuciferine, glaziovine[ 65] [ 74]
Homoaporphines[ 80]
Kreysiginine, multifloramine[ 80]
Homoproaporphines[ 80]
Bulbocodine[ 72]
Morphines [ 81] 모르핀 , 코데인 , 테바인 , 시노메닌 [ 82]
Homomorphines[ 83]
Kreysiginine, androcymbine[ 81]
Tropoloisoquinolines[ 65]
Imerubrine[ 65]
Azofluoranthenes[ 65]
Rufescine, imeluteine[ 84]
아마릴리스 알칼로이드[ 85] 리코린 , ambelline, 타제틴, 갈란타민 , montanine[ 86]
Erythrite alkaloids[ 69] 에리소딘, 에리트로이딘[ 69]
페난트렌 계(Phenanthrene-)[ 65] Atherosperminine[ 65] [ 75]
Protopins [ 65] 프로토핀 (Protopine), oxomuramine, corycavidine[ 78]
Aristolactam[ 65]
Doriflavin[ 65]
옥사졸 계[ 87]
티로신 → 티라민 [ 88] Annuloline, halfordinol, texaline, texamine[ 89]
이소옥사졸 계(Isoxazole-)
이보텐산 (Ibotenic acid) → 무시몰 (Muscimol)
이보텐산, 무시몰
티아졸 계(Thiazole-)[ 90]
1-디옥시-D-크실룰로오스 5-인산염 (DOXP), 티로신 , 시스테인 [ 91] Nostocyclamide, 티오스트렙톤(thiostreptone)[ 90] [ 92]
퀴나졸린 계(Quinazoline-)[ 93] 3,4-다이하이드로-4-퀴나졸린계
안트라닐산 (Anthranilic acid) 또는 페닐알라닌 또는 오르니틴 [ 94] Febrifugine [ 95]
1,4-다이하이드로-4-퀴나졸린계
글리코린(Glycorine), arborine, glycosminine[ 95]
피롤리딘 및 피페르딘 퀴나졸린계
페가닌 (peganine)[ 87]
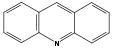
아크리딘 계(Acridine-)[ 87]
안트라닐산 (Anthranilic acid)[ 96] Rutacridone, 아크로니신 (acronicine)[ 97] [ 98]
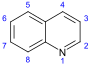
퀴놀린 계(Quinoline-)[ 99] [ 100] Simple derivatives of quinoline derivatives of 2 - quinolones and 4-quinolone
안트라닐산 → 3-카르복시퀴놀린[ 101] Cusparine, echinopsine , evocarpine[ 100] [ 102] [ 103]
Tricyclic terpenoids
Flindersine[ 100] [ 104]
Furanoquinoline계
딕탐닌 , 파가린, 스킴미아닌(β-파가린)[ 100] [ 105] [ 106]
Quinines
트립토판 → 트립타민 → 스트릭토시딘 (세콜로가닌 과 함께) → korinanteal → cinhoninon [ 67] [ 101] 퀴닌 , 퀴니딘 , 신코닌 , cinhonidine[ 104]
인돌 계[ 82] 무(無)이소프렌 인돌알칼로이드
단순 인돌계 물질[ 107]
트립토판 → 트립타민 또는 5-하이드록시트립토판[ 108] 세로토닌 , 실로시빈 , 디메틸트립타민 (DMT), 부포테닌 [ 109] [ 110]
단순 β-카르볼린 계 물질[ 111]
하르만, 하르민 , 하르말린 , 엘레아그닌[ 107]
피롤로인돌알칼로이드(Pyrroloindole-)[ 112]
피소스티그민 (에세린), etheramine, physovenine, 엡타스티그민(eptastigmine)[ 112]
준(準)테르페노이드 인돌알칼로이드
맥각알칼로이드 (Ergot alkaloids)[ 82] 트립토판 → chanoclavine → 아그로클라빈(agroclavine) → 엘리모클라빈(elimoclavine) → paspalic acid → 리세르그산 (lysergic acid)[ 112] 에르고타민 (Ergotamine), 에르고바신(ergobasine), ergosine[ 113]
모노테르페노이드 인돌알칼로이드
Corynanthe type alkaloids[ 108] 트립토판 → 트립타민 → 스트릭토시딘 (세콜로가닌 과 함께)[ 108] 아즈말리신(Ajmalicine), 사르파긴(sarpagine), 보바신(vobasine), 아즈말린 (ajmaline), 요힘빈 (yohimbine), 레세르핀 (reserpine), 미트라기닌 (mitragynine),[ 114] [ 115] strychnine and (Strychnine brucine , aquamicine, vomicine [ 116]
이보가 형(Iboga-type) 알칼로이드[ 108] Ibogamine , ibogaine , voacangine [ 108]
아스피도스페르마 형(Aspidosperma-type) 알칼로이드[ 108] 빈카민 , 빈코틴, 아스피도스페르민[ 117] [ 118]
이미다졸 계(Imidazole-)[ 87]
히스티딘 (histidine)에서 직접[ 119] 히스타민 , 필로카르핀(pilocarpine), pilosine, stevensine[ 87] [ 119]
푸린 계[ 120]
크산토신 (푸린 생합성 중에 생김) → 7 메틸크산토신 → 7-메틸 크산틴 → 테오브로민 → 카페인 [ 67] 카페인 , 테오브로민 , 테오필린 , 색시토신 (saxitoxin)[ 121] [ 122]
곁사슬에 질소를 가진 알칼로이드 (원시알칼로이드)
β-페닐에틸아민 계[ 74]
티롭신 또는 페닐알라닌 → 디옥시페닐알라닌 → 도파민 → 아드레날린 , 메스칼린 , 티로신 → 티라민 페닐알라닌 → 1-페닐프로판-1,2-디온 → 카티논 (cathinone) → 에페드린 및 슈도에페드린 (pseudoephedrine)[ 11] [ 34] [ 123] 티라민 , 에페드린 , 슈도에페드린 , 메스칼린 , 카티논 , 카테콜아민 (catecholamines) (아드레날린 , 노르아드레날린 (noradrenaline), 도파민 )[ 11] [ 124]
콜히친 알칼로이드[ 125]
티로신 또는 페닐알라닌 → 도파민 → autumnaline → 콜히친 [ 126] 콜히친 , colchamine[ 125]
Muscarine [ 127]
글루탐산 → 3-케토글루탐산 → 무스카린 (피루브산 과 같이)[ 128] 무스카린 , 알로무스카린(allomuscarine), 에피무스카린(epimuscarine), 에피알로무스카린(epiallomuscarine)[ 127]
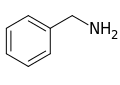
Benzylamine[ 129]
페닐알라닌 및 발린 , 류신 또는 이소류신 [ 130] 캅사이신 , 디하이드로캅사이신 , 노르디하이드로캅사이신[ 129] [ 131]
폴리아민 알칼로이드
푸트레신 계[ 132]
오르니틴 → 푸트레신 → 스페르미딘 → 스페르민 [ 133] Paucine[ 132]
스페르미딘 계[ 132]
Lunarine, codonocarpine[ 132]
스페르민 계[ 132]
Verbascenine, aphelandrine[ 132]
펩타이드(사이클로펩타이드) 알칼로이드
Peptide alkaloids with a 13-membered cycle[ 30] [ 134]
Numularine C type
From different amino acids[ 30]
Numularine C, numularine S[ 30]
Ziziphin type
Ziziphin A, sativanine H[ 30]
Peptide alkaloids with a 14-membered cycle[ 30] [ 134]
Frangulanine type
Frangulanine, scutianine J[ 134]
Scutianine A type
Scutianine A[ 30]
Integerrine type
Integerrine, discarine D[ 134]
Amphibine F type
Amphibine F, spinanine A[ 30]
Amphibine B type
Amphibine B, lotusine C[ 30]
Peptide alkaloids with a 15-membered cycle[ 134]
Mucronine A type
Mucronine A[ 134] [ 135]
유사알칼로이드 (테르펜 및 스테로이드 )
디테르펜(Diterpenes)[ 135]
Licoctonine type
메발론산 (Mevalonic acid) → izopentenilpyrophosfate → geranyl pyrophosphate [ 136] [ 137] 아코니틴 (Aconitine), 델피닌 (delphinine)[ 135] [ 138]
스테로이드 [ 139]
콜레스테롤 , 아르기닌 [ 140] 솔라소딘(solasodine), 솔라니딘 (solanidine), veralkamine[ 141]
어미양이 익시아 (Veratrum californicum )의 잎을 먹고 낳은 기형 새끼양. 이 식물에 들어있는 알칼로이드인 사이클로파민 은 눈이 하나 밖에 없는 키클로푸스증 을 유발할 수 있다.[ 142] 대부분 알칼로이드는 산소를 가지며 공기 중에서 무색 결정이 된다. 산소를 포함하지 않는 니코틴 [ 143] 코닌 [ 20] [ 144] 베르베린 과 상귀나린 같은 알칼로이드는 노란 계열의 색을 띠기도 한다.[ 144]
다양한 종류의 살아있는 생물체가 알칼로이드를 생산 하며, 특히 관다발식물 의 경우 10~25%의 종이 알칼로이드를 포함하고 있다.[ 145] [ 146] [ 147]
대개 식물에 포함된 알칼로이드는 몇 %이상을 넘지 않으며 당연히 조직 전반에 균질하지도 않다. 알칼로이드가 집중된 곳은 식물에 따라 잎(사리풀 ), 열매나 씨(스트리키니네 ), 뿌리(인도사목 ), 껍질(기나나무 ) 등으로 다르며,[ 148] [ 149]
알칼로이드는 식물 뿐 아니라, 환각버섯속 (Psilocybe)의 버섯종에서 얻는 실로시빈 처럼 특정 균류 에서도, 일부 두꺼비의 피부에 존재하는 독성 알칼로이드 부포테닌 처럼 동물에서도 발견된다.[ 13] [ 150] 아드레날린 이나 세로토닌 따위의 아민 은 구조면이나 생합성 과정이 알칼로이드와 유사하며 고등생물에서 중요한 역할을 수행하는데, 이들을 알칼로이드라 부르기도 한다.[ 151]
↑ Andreas Luch (2009). 《Molecular, clinical and environmental toxicology》. Springer. 20쪽. ISBN 3764383356 ↑ 가 나 IUPAC. Compendium of Chemical Terminology , 2판. (The "Gold Book"). A. D. McNaught, A. Wilkinson 편집. Blackwell Scientific Publications, 옥스포드 (1997) ISBN 0-9678550-9-8 doi :10.1351/goldbook ↑ R. H. F. Manske. The Alkaloids. Chemistry and Physiology . Volume VIII. - 뉴욕: Academic Press, 1965, p. 673
↑ Robert Alan Lewis (1998). 《ISBN 1-56670-223-2 ↑ 가 나 다 라 Chemical Encyclopedia: alkaloids ↑ Rhoades, David F (1979). 〈Evolution of Plant Chemical Defense against Herbivores〉. Rosenthal, Gerald A., and Janzen, Daniel H. 《Herbivores: Their Interaction with Secondary Plant Metabolites》 . 뉴욕: Academic Press. 41 쪽. ISBN 0-12-597180-X ↑ Robert A. Meyers Encyclopedia of Physical Science and Technology , 3판 중 Alkaloids 항목. ISBN 0-12-227411-3
↑ Leland J. Cseke, Natural Products from Plants . Second Edition. - CRC, 2006, p. 30 ISBN 0-8493-2976-0
↑ A. William Johnson. Invitation to Organic Chemistry , Jones and Bartlett, 1999, 433쪽 ISBN 0-7637-0432-6
↑ Raj K Bansal, A Text Book of Organic Chemistry . 4판, New Age International, 2004, 644쪽 ISBN 81-224-1459-1
↑ 가 나 다 라 Aniszewski, 110쪽
↑ Hesse, 1~3쪽
↑ 가 나 Hesse, 5쪽
↑ Hesse, 7쪽
↑ Aniszewski, 182쪽
↑ Hesse, 338쪽
↑ Hesse, 304쪽
↑ Hesse, 350쪽
↑ Hesse, 313~316쪽
↑ 가 나 TSB: Coniine [깨진 링크 (과거 내용 찾기 )] ↑ Hesse, 204쪽
↑ 가 나 Hesse, 11쪽
↑ Orekhov, 6쪽
↑ Aniszewski, 109쪽
↑ Dewick, 307쪽
↑ Hesse, 12쪽
↑ 가 나 Plemenkov, 223쪽
↑ 가 나 Hesse, 31쪽
↑ 가 나 다 Dewick, 381쪽
↑ 가 나 다 라 마 바 사 아 자 Dimitris C. Gournelif, Gregory G. Laskarisb and Robert Verpoorte (1997). “Cyclopeptide alkaloids”. 《Nat. Prod. Rep.》 14 (1): 75~82. doi :10.1039/NP9971400075 . PMID 9121730 . ↑ Aniszewski, 11쪽
↑ Plemenkov, 246쪽
↑ 가 나 Aniszewski, 12쪽
↑ 가 나 Dewick, 382쪽
↑ Hesse, 44, 53쪽
↑ 가 나 다 Plemenkov, 224쪽
↑ 가 나 다 Aniszewski, 75쪽
↑ Orekhov, 33쪽
↑ 가 나 다 Chemical Encyclopedia: Tropan alkaloids ↑ Hesse, 34쪽
↑ Aniszewski, 27쪽
↑ 가 나 다 라 Chemical Encyclopedia: Pyrrolizidine alkaloids ↑ Plemenkov, 229쪽
↑ Blankenship JD, Houseknecht JB, Pal S, Bush LP, Grossman RB, Schardl CL (2005). “Biosynthetic precursors of fungal pyrrolizidines, the loline alkaloids”. 《Chembiochem》 6 (6): 1016~1022. doi :10.1002/cbic.200400327 . PMID 15861432 . ↑ Faulkner JR, Hussaini SR, Blankenship JD, Pal S, Branan BM, Grossman RB, Schardl CL (2006). “On the sequence of bond formation in loline alkaloid biosynthesis”. 《Chembiochem》 7 (7): 1078~1088. doi :10.1002/cbic.200600066 . PMID 16755627 . ↑ Schardl CL, Grossman RB, Nagabhyru P, Faulkner JR, Mallik UP (2007). “Loline alkaloids: currencies of mutualism”. 《Phytochemistry 》 68 (7): 980–996. doi :10.1016/j.phytochem.2007.01.010 . PMID 17346759 . ↑ Plemenkov, 225쪽
↑ Aniszewski, 95쪽
↑ Orekhov, 80쪽
↑ 가 나 다 라 마 바 Chemical Encyclopedia: Quinolizidine alkaloids ↑ Saxton, 1권, 93쪽
↑ Aniszewski, 98쪽
↑ Saxton, 91쪽
↑ Joseph P. Michael (2002). “Indolizidine and quinolizidine alkaloids”. 《Nat. Prod. Rep》 19 : 458~475. doi :10.1039/b208137g . ↑ Saxton, 1권, 92쪽
↑ Dewick, 310쪽
↑ Aniszewski, 96쪽
↑ Aniszewski, 97쪽
↑ 가 나 다 Plemenkov, 227쪽
↑ 가 나 Chemical Encyclopedia: pyridine alkaloids ↑ 가 나 Aniszewski, 107쪽
↑ 가 나 Aniszewski, 85쪽
↑ Plemenkov, 228쪽
↑ 가 나 Hesse, 36쪽
↑ 가 나 다 라 마 바 사 아 자 차 카 타 파 하 거 너 더 러 머 버 Chemical Encyclopedia: isoquinoline alkaloids ↑ Aniszewski, 77~78쪽
↑ 가 나 다 Tadhg P. Begley. Encyclopedia of Chemical Biology: Alkaloid Biosynthesis↑ 가 나 Saxton, 3권, 122쪽
↑ 가 나 다 Hesse, p. 54
↑ 가 나 Hesse, p. 37
↑ Hesse, p. 38
↑ 가 나 다 Hesse, p. 46
↑ 가 나 다 Hesse, p. 50
↑ 가 나 다 Kenneth W. Bentley (1997). “β-Phenylethylamines and the isoquinoline alkaloids”. 《Nat. Prod. Rep》 14 (4): 387–411. doi :10.1039/NP9971400387 . PMID 9281839 . ↑ 가 나 Hesse, p. 47
↑ Hesse, p. 39
↑ 가 나 Hesse, p. 41
↑ 가 나 Hesse, p. 49
↑ Hesse, p. 44
↑ 가 나 다 Saxton, 3권, 164쪽
↑ 가 나 Hesse, 51쪽
↑ 가 나 다 Plemenkov, 236쪽
↑ Saxton, 3권, 163쪽
↑ Saxton, 3권, 168쪽
↑ Hesse, 52쪽
↑ Hesse, 53쪽
↑ 가 나 다 라 마 Plemenkov, p. 241
↑ Arnold Brossi The Alkaloids: Chemistry and Pharmacology , Volume 35. - Academic Press, 1989, p. 261
↑ Arnold Brossi The Alkaloids: Chemistry and Pharmacology , Volume 35. - Academic Press, 1989, pp. 260–263
↑ 가 나 Plemenkov, p. 242
↑ Tadhg P. Begley. Encyclopedia of Chemical Biology: Cofactor Biosynthesis↑ John R. Lewis (2000). “Amaryllidaceae, muscarine, imidazole, oxazole, thiazole and peptide alkaloids, and other miscellaneous alkaloids” . 《Nat. Prod. Rep》 17 (1): 57–84. doi :10.1039/a809403i . PMID 10714899 . ↑ Chemical Encyclopedia: Quinazoline alkaloids ↑ Aniszewski, p. 106
↑ 가 나 Aniszewski, p. 105
↑ Richard B. Herbert; Herbert, Richard B.; Herbert, Richard B. (1999). “The biosynthesis of plant alkaloids and nitrogenous microbial metabolites” . 《Nat. Prod. Rep》 16 : 199~208. doi :10.1039/a705734b . ↑ Plemenkov, pp. 231, 246
↑ Hesse, p. 58
↑ Plemenkov, p. 231
↑ 가 나 다 라 Chemical Encyclopedia: Quinoline alkaloids ↑ 가 나 Aniszewski, p. 114
↑ Orekhov, p. 205
↑ Hesse, p. 55
↑ 가 나 Plemenkov, p. 232
↑ Orekhov, p. 212
↑ Aniszewski, p. 118
↑ 가 나 Aniszewski, 112쪽
↑ 가 나 다 라 마 바 Aniszewski, p. 113
↑ Hesse, 15쪽
↑ Saxton, 1권, 467쪽
↑ Dewick, p. 349-350
↑ 가 나 다 Aniszewski, p. 119
↑ Hesse, p. 29
↑ Hesse, pp. 23-26
↑ Saxton, 1권, 169쪽
↑ Saxton, 5권, 210쪽
↑ Hesse, pp. 17-18
↑ Dewick, p. 357
↑ 가 나 Aniszewski, p. 104
↑ Hesse, p. 72
↑ Hesse, p. 73
↑ Dewick, p. 396
↑ “PlantCyc Pathway: ephedrine biosynthesis” . 2011년 12월 10일에 원본 문서 에서 보존된 문서. 2010년 6월 6일에 확인함 . ↑ Hesse, p. 76
↑ 가 나 Chemical Encyclopedia: colchicine alkaloids ↑ Aniszewski, 77쪽
↑ 가 나 Hesse, p. 81
↑ Arnold Brossi The Alkaloids: Chemistry and Pharmacology , Volume 23. - Academic Press, 1984, p. 376
↑ 가 나 Hesse, p. 77
↑ Arnold Brossi The Alkaloids: Chemistry and Pharmacology , Volume 23. - Academic Press, 1984, p. 268
↑ Arnold Brossi The Alkaloids: Chemistry and Pharmacology , Volume 23. - Academic Press, 1984, p. 231
↑ 가 나 다 라 마 바 Hesse, p. 82
↑ Spermine Biosynthesis ↑ 가 나 다 라 마 바 Plemenkov, p. 243
↑ 가 나 다 Hesse, p. 84
↑ Chemical Encyclopedia: Terpenes ↑ Tadhg P. Begley. Encyclopedia of Chemical Biology: Natural Products: An Overview↑ Atta-ur-Rahman and M. Iqbal Choudhary (1997). “Diterpenoid and steroidal alkaloids” . 《Nat. Prod. Rep》 14 (2): 191~203. doi :10.1039/np9971400191 . PMID 9149410 . ↑ Hesse, p. 88
↑ Dewick, p. 388
↑ Plemenkov, p. 247
↑ Cancer Drug Behind Cyclops Birth? , 와이어드 뉴스, 2006년 8월 14일↑ “TSB: Nicotine” . 2012년 7월 22일에 원본 문서 에서 보존된 문서. 2012년 2월 19일에 확인함 . ↑ 가 나 Grinkevich, p. 131
↑ Aniszewski, 13쪽
↑ Orekhov, 11쪽
↑ Hesse, p.4
↑ Grinkevich, 122~123쪽
↑ Orekhov, 12쪽
↑ Fattorusso, p. XVII
↑ Aniszewski, 110~111쪽
Tadeusz Aniszewski (2007). 《Alkaloids - secrets of life 》(알칼로이드, 생명의 비밀) Amsterdam: Elsevier. ISBN 978-0-444-52736-3 .
Paul M Dewick (2002). 《Medicinal Natural Products. A Biosynthetic Approach 》 Wiley. 제2판. ISBN 0-471-49640-5 .
Manfred Hesse (2002). 《Alkaloids: Nature's Curse or Blessing? 》(알칼로이드: 자연의 저주? 아니면 축복?) Wiley-VCH. ISBN 978-3-906390-24-6 .
Orekhov AP (1955). 《Chemistry alkaloids 》(알칼로이드 화학) Acad. 제2판. M.: USSR.
Plemenkov VV (2001). 《Introduction to the Chemistry of Natural Compounds 》(천연화합물 화학 개론) Kazan.
J. E. Saxton (1973). 《The Alkaloids. A Specialist Periodical Report 》 - 런던: The Chemical Society.