–ü–ª—É—Ç–æ–Ω–∏—ò—É–º –ò–º–µ, —Å–∏–º–±–æ–ª –ø–ª—É—Ç–æ–Ω–∏—ò—É–º, Pu –ò–∑–≥–ª–µ–¥ —Å—Ä–µ–±—Ä–Ω–∞—Å—Ç–æ –±–µ–æ, –ø–æ—Ç–∞–º—ö—É—ò–µ –¥–æ —Ç–∞–º–Ω–æ —Å–∏–≤–µ –Ω–∞ –≤–∞–∑–¥—É—Ö—É
–ê—Ç–æ–º—Å–∫–∏ –±—Ä–æ—ò (Z ) 94 –ì—Ä—É–ø–∞ , –ø–µ—Ä–∏–æ–¥–∞ –≥—Ä—É–ø–∞ –ù/–î , –ø–µ—Ä–∏–æ–¥–∞ 7 –ë–ª–æ–∫ f-–±–ª–æ–∫ –ö–∞—Ç–µ–≥–æ—Ä–∏—ò–∞ –∞–∫—Ç–∏–Ω–æ–∏–¥ –Ý–µ–ª. –∞—Ç. –º–∞—Å–∞ (A r ) 244,0642053(56)[ 1] –ú–∞—Å–µ–Ω–∏ –±—Ä–æ—ò 244 (–Ω–∞—ò—Å—Ç–∞–±–∏–ª–Ω–∏—ò–∏ –∏–∑–æ—Ç–æ–ø) –ï–ª. –∫–æ–Ω—Ñ–∏–≥—É—Ä–∞—Ü–∏—ò–∞ –ø–æ —ô—É—Å–∫–∞–º–∞
2, 8, 18, 32, 24, 8, 2 Тачка топљења 912,5 K ​(639,4 °‍C , ​1182,9 °F) Тачка кључања 3505 K ​(3228 °‍C , ​5842 °F) Густина при с.т. 19,816 g/cm3 течно ст., на т.т. 16,63 g/cm3 Топлота фузије 2,82 kJ/mol Топлота испаравања 333,5 kJ/mol Мол. топл. капацитет 35,5 J/(mol·K) Напон паре
P (Pa)
100
101
102
–Ω–∞ T (K)
1756
1953
2198
P (Pa)
103
104
105
–Ω–∞ T (K)
2511
2926
3499
Електронегативност 1,28 Енергије јонизације 1 : 584,7 kJ/mol Атомски радијус 159 pm Ковалентни радијус 187±1 pm Спектралне линије Кристална структура ​моноклинична Брзина звука 2260 m/s Топл. ширење 46,7 µm/(m·K) (на 25 °‍C ) Топл. водљивост 6,74 W/(m·K) Електроотпорност 1,460 µΩ·m (на 0 °‍C ) Магнетни распоред парамагнетичан Јангов модул 96 GPa Модул смицања 43 GPa Поасонов коефицијент 0,21 CAS број 7440-07-5 Именовање по патуљастој планети Плутону , који је именован по класичном богу подземља Плутону Откриће Глен Т. Сиборг , Артур Вал , Џозеф Кенеди , Едвин Макмилан (1940–1)
референце • Википодаци
–ü–ª—É—Ç–æ–Ω–∏—ò—É–º (Pu , –ª–∞—Ç. plutonium —Ö–µ–º–∏—ò—Å–∫–∏ –µ–ª–µ–º–µ–Ω—Ç –∏–∑ –≥—Ä—É–ø–µ –∞–∫—Ç–∏–Ω–æ–∏–¥–∞ .[ 2] –ü–ª—É—Ç–æ–Ω—É .
–ü–ª—É—Ç–æ–Ω–∏—ò—É–º —ò–µ —Ä–∞–¥–∏–æ–∞–∫—Ç–∏–≤–∞–Ω –º–µ—Ç–∞–ª –∏–∑ –≥—Ä—É–ø–µ –∞–∫—Ç–∏–Ω–æ–∏–¥–∞.[ 3] –∞–º–µ—Ä–∏—á–∫–æ–≥ —Ö–µ–º–∏—á–∞—Ä–∞ –ì–ª–µ–Ω–∞ –°–∏–±–æ—Ä–≥–∞ 1941 . –≥–æ–¥–∏–Ω–µ. –ù–∞—É—á–Ω–∏—Ü–∏ —Å—É –∏—Å–∫–æ—Ä–∏—Å—Ç–∏–ª–∏ —É—Ä–∞–Ω–∏—ò—É–º , –∫–æ—ò–∏ —Å—É –±–æ–º–±–∞—Ä–¥–æ–≤–∞–ª–∏ —ò–µ–∑–≥—Ä–∏–º–∞ –¥–µ—É—Ç–µ—Ä–∏—ò—É–º–∞ (–∏–∑–æ—Ç–æ–ø –≤–æ–¥–æ–Ω–∏–∫–∞ ). –ü–ª—É—Ç–æ–Ω–∏—ò—É–º —ò–µ –≤–µ–æ–º–∞ —Ä–µ–∞–∫—Ç–∏–≤–∞–Ω. –ê–∫–æ –¥—É–≥–æ —Å—Ç–æ—ò–∏ –Ω–∞ –≤–∞–∑–¥—É—Ö—É –ø—Ä–µ–∫—Ä–∏–≤–∞ —Å–µ –∑–ª–∞—Ç–Ω–∏–º —Å–ª–æ—ò–µ–º –æ–∫—Å–∏–¥–∞. –à–∞–≤—ô–∞ —Å–µ —É 6 –∞–ª–æ—Ç—Ä–æ–ø—Å–∫–∏—Ö –º–æ–¥–∏—Ñ–∏–∫–∞—Ü–∏—ò–∞ –∏ –≥—Ä–∞–¥–∏ —ò–µ–¥–∏—ö–µ—ö–∞ —É –∫–æ—ò–∏–º–∞ —Å–µ —ò–∞–≤—ô–∞ —Å–∞ —á–µ—Ç–∏—Ä–∏ –æ–∫—Å–∏–¥–∞—Ü–∏–æ–Ω–∞ –±—Ä–æ—ò–∞ . –ü–æ–∑–Ω–∞—Ç–æ —ò–µ 15 –∏–∑–æ—Ç–æ–ø–∞ –ø–ª—É—Ç–æ–Ω–∏—ò—É–º–∞ —á–∏—ò–µ —Å–µ –∞—Ç–æ–º—Å–∫–µ –º–∞—Å–µ –∫—Ä–µ—õ—É –∏–∑–º–µ—í—É 232 –∏ 246. –ó–±–æ–≥ –≤–∏—Å–æ–∫–æ–≥ —Å—Ç–µ–ø–µ–Ω–∞ —Ä–∞–¥–∏–æ–∞–∫—Ç–∏–≤–Ω–æ—Å—Ç–∏ —Å–º—Ä—Ç–æ–Ω–æ—Å–∞–Ω —ò–µ –∑–∞ —á–æ–≤–µ–∫–∞ —á–∞–∫ –∏ —É –º–∏–Ω–∏–º–∞–ª–Ω–∏–º –∫–æ–ª–∏—á–∏–Ω–∞–º–∞. –û–ø–∞—Å–Ω–∏—ò–∏ —ò–µ –æ–¥ —É—Ä–∞–Ω–∏—ò—É–º–∞ –∑–±–æ–≥ –º–∞—ö–µ –∫—Ä–∏—Ç–∏—á–Ω–µ –º–∞—Å–µ.
–ü—Ä–µ–º–∞ —Å–≤–æ–º —Ä–µ–¥–Ω–æ–º –±—Ä–æ—ò—É, –æ–Ω —ò–µ –Ω–∞—ò—Ç–µ–∂–∏ –µ–ª–µ–º–µ–Ω—Ç –∫–æ—ò–∏ —Å–µ –Ω–∞–ª–∞–∑–∏ —É –ø—Ä–∏—Ä–æ–¥–∏. –ú–µ—í—É—Ç–∏–º, —É –ø—Ä–∏—Ä–æ–¥–∏ —Å–µ –Ω–∞–ª–∞–∑–∏ —Å–∞–º–æ —É —Ç—Ä–∞–≥–æ–≤–∏–º–∞ —É–Ω—É—Ç–∞—Ä –≤–µ–æ–º–∞ —Å—Ç–∞—Ä–∏—Ö —Å—Ç–µ–Ω–∞. –¢—Ä–∞–≥–æ–≤–∏ –æ–≤–æ–≥ –µ–ª–µ–º–µ–Ω—Ç–∞ —Å–µ —ò–∞–≤—ô–∞—ò—É –º–µ—í—É —Ä—É–¥–∞–º–∞ —É—Ä–∞–Ω–∏—ò—É–º–∞. –í–µ—õ–µ –∫–æ–ª–∏—á–∏–Ω–µ –æ–≤–æ–≥ –µ–ª–µ–º–µ–Ω—Ç–∞ –¥–æ–±–∏—ò–∞—ò—É —Å–µ –≤–µ—à—Ç–∞—á–∫–∏, –ø—Ä–µ—Ç–µ–∂–Ω–æ —É –∞—Ç–æ–º—Å–∫–∏–º —Ü–µ–Ω—Ç—Ä–∞–ª–∞–º–∞ –∏ —Ä–µ–∞–∫—Ç–æ—Ä–∏–º–∞. –ö–∞–æ —ò–µ–¥–∞–Ω –æ–¥ –º–∞–ª–æ–±—Ä–æ—ò–Ω–∏—Ö —Ö–µ–º–∏—ò—Å–∫–∏—Ö –µ–ª–µ–º–µ–Ω–∞—Ç–∞ –ø–æ–¥–ª–æ–∂–Ω–∏—Ö —Ñ–∏—Å–∏—ò–∏, –∏–≥—Ä–∞ –≤–µ–æ–º–∞ –≤–∞–∂–Ω—É —É–ª–æ–≥—É –∑–∞ –ø—Ä–æ–∏–∑–≤–æ–¥—ö—É –Ω—É–∫–ª–µ–∞—Ä–Ω–æ–≥ –æ—Ä—É–∂—ò–∞ . –ù–∞ –ø—Ä–∏–º–µ—Ä, –æ—Å–Ω–æ–≤–Ω–∏ —Ä–µ–∞–∫—Ç–∏–≤–Ω–∏ –º–∞—Ç–µ—Ä–∏—ò–∞–ª —É –∞—Ç–æ–º—Å–∫–æ—ò –±–æ–º–±–∏ –±–∞—á–µ–Ω–æ—ò 9. –∞—É–≥—É—Å—Ç–∞ 1945. –Ω–∞ –ù–∞–≥–∞—Å–∞–∫–∏ –±–∏–æ —ò–µ –ø–ª—É—Ç–æ–Ω–∏—ò—É–º. –û–≤–∞—ò –µ–ª–µ–º–µ–Ω—Ç –Ω–∞—Å—Ç–∞—ò–µ —Ç–æ–∫–æ–º —Ä–∞–¥–∞ –Ω—É–∫–ª–µ–∞—Ä–Ω–∏—Ö —Ä–µ–∞–∫—Ç–æ—Ä–∞ –∏–∑ —É—Ä–∞–Ω–∏—ò—É–º—Å–∫–∏—Ö —à–∏–ø–∫–∏ –Ω—É–∫–ª–µ–∞—Ä–Ω–æ–≥ –≥–æ—Ä–∏–≤–∞.
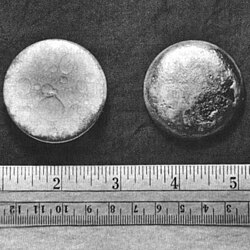
–ü–ª–æ—á–∞ –ø–ª—É—Ç–æ–Ω–∏—ò—É–º–∞ –Ω–∞ –±–ª–æ–∫—É –æ–¥ –∫–∞–ª—Ü–∏—ò—É–º —Ö–ª–æ—Ä–∏–¥–∞. –ü–ª—É—Ç–æ–Ω–∏—ò—É–º –ü–ª—É—Ç–æ–Ω–∏—ò—É–º —Å—É –æ—Ç–∫—Ä–∏–ª–∏ –∞–º–µ—Ä–∏—á–∫–∏ –Ω–∞—É—á–Ω–∏—Ü–∏ –ì–ª–µ–Ω –¢. –°–∏–±–æ—Ä–≥ , –ê—Ä—Ç—É—Ä –í–∞–ª , –è–æ–∑–µ—Ñ –ö–µ–Ω–µ–¥–∏ , –ú–∞—ò–∫–ª –ö–µ—Ñ–æ–ª–∞ –∏ –ï–¥–≤–∏–Ω –ú–∞–∫–º–∏–ª–∞–Ω . –û–Ω–∏ —Å—É 14. –¥–µ—Ü–µ–º–±—Ä–∞ 1940. –∏–∑–≤–µ–ª–∏ –µ–∫—Å–ø–µ—Ä–∏–º–µ–Ω—Ç —É —Ü–∏–∫–ª–æ—Ç—Ä–æ–Ω—É , –±–æ–º–±–∞—Ä–¥—É—ò—É—õ–∏ –º–µ—Ç—É –æ–¥ —É—Ä–∞–Ω–∏—ò—É–º–∞ 238 U –∞—Ç–æ–º–∏–º–∞ –¥–µ—É—Ç–µ—Ä–∏—ò—É–º–∞ –¥–æ–±–∏–≤—à–∏ —Ç–∞–∫–æ –∏–∑–æ—Ç–æ–ø 238 Pu. –ü—Ä–∏ —Ç–æ–º –µ–∫—Å–ø–µ—Ä–∏–º–µ–Ω—Ç—É, –Ω–∞—ò–ø—Ä–µ —ò–µ –Ω–∞–ø—Ä–∞–≤—ô–µ–Ω —É–∑–æ—Ä–∞–∫ 238 U —É –æ–±–ª–∏–∫—É –æ–∫—Å–∏–¥–∞ U3 O8 —É —Ç–∞–Ω–∫–æ–º —Å–ª–æ—ò—É –Ω–∞ –ø–ª–æ—á–∏ –æ–¥ –±–∞–∫—Ä–∞. –£ –æ–≤–æ—ò —Ä–µ–∞–∫—Ü–∏—ò–∏ –µ–º–∏—Ç–æ–≤–∞–Ω–∞ —Å—É –¥–≤–∞ –Ω–µ—É—Ç—Ä–æ–Ω–∞ . –£–∫—Ä–∞—Ç–∫–æ –Ω–∞–∫–æ–Ω —Ç–æ–≥–∞, –Ω–∞—Å—Ç–∞–æ —ò–µ –Ω–µ–ø—Ç—É–Ω–∏—ò—É–º –∫–∞–æ –º–µ—í—É–ø—Ä–æ–∏–∑–≤–æ–¥, –∫–æ—ò–∏ —Å–µ –æ–¥–º–∞—Ö —Ä–∞—Å–ø–∞–æ –Ω–∞ 238 Pu. –ù–µ–¥–≤–æ—Å–º–∏—Å–ª–µ–Ω–∏ –¥–æ–∫–∞–∑ –æ –¥–æ–±–∏—ò–∞—ö—É –µ–ª–µ–º–µ–Ω—Ç–∞ 94 –¥–∞–æ —ò–µ –ê—Ä—Ö—É—Ä –í–∞–ª 23/24. —Ñ–µ–±—Ä—É–∞—Ä–∞ 1941. –≥–æ–¥–∏–Ω–µ.[ 4] [ 5]
92
238
U
+
1
2
D
‚ü∂
93
238
N
p
+
2
0
1
n
;
93
238
N
p
‚Üí
2
,
117
d
β
‚àí
94
238
P
u
{\displaystyle \mathrm {^{238}_{\ 92}U\ +\ _{1}^{2}D\ \longrightarrow \ _{\ 93}^{238}Np\ +\ 2\ _{0}^{1}n\quad ;\quad _{\ 93}^{238}Np\ {\xrightarrow[{2,117\ d}]{\beta ^{-}}}\ _{\ 94}^{238}Pu} }
–î—Ä—É–≥–∏ –∏–∑–æ—Ç–æ–ø –ø–ª—É—Ç–æ–Ω–∏—ò—É–º–∞ –¥–æ–±–∏—ò–µ–Ω —ò–µ –±–æ–º–±–∞—Ä–¥–æ–≤–∞—ö–µ–º –±—Ä–∑–∏–º –Ω–µ—É—Ç—Ä–æ–Ω–∏–º–∞:
92
238
U
+
0
1
n
‚ü∂
92
239
U
‚Üí
23
,
5
m
i
n
β
‚àí
93
239
N
p
‚Üí
2
,
3565
d
β
‚àí
94
239
P
u
{\displaystyle \mathrm {^{238}_{\ 92}U\ +\ _{0}^{1}n\ \longrightarrow \ _{\ 92}^{239}U\ {\xrightarrow[{23,5\ min}]{\beta ^{-}}}\ _{\ 93}^{239}Np\ {\xrightarrow[{2,3565\ d}]{\beta ^{-}}}\ _{\ 94}^{239}Pu} }
Наведена времена су времена полураспада. Новооткривеном елементу је дато име у марту 1942. године по у то време најудаљенијој откривеној планети Плутону , а која је опет добила име по истоименом божанству из римске митологије: …назван по планети која следи након Нептуна, а у аспекту ужасавајућег деловања плутонијумске атомске бомбе далеко више му одговара извођење из имена Плутона, божанства подземља . Према томе, три дотад најтежа позната елемента, уранијум, нептунијум и плутонијум добили су имена према истоименим планетама: Урану , Нептуну и Плутону. Прва мерљива количина плутонијума од око 4 µg добијена је у августу/септембру 1942. када ју је изоловала група научника Барис Канингам , Мајкл Кефола и Луис Вернер .[ 7] Другог светског рата . Са првом производњом плутонијума у већем обиму отпочело се у оквирима америчког пројекта „Менхетн”. Прва експлозија атомске бомбе којој је сведочило човечанство био је тест „Тринити”, чија је основа био плутонијум 239 Pu, као и за бомбу Дебељко ((језик: енглески) ) која је у августу 1945. разорила јапански град Нагасаки. Џозеф Хамилтон је изводио тестове на добровољцима, дајући им плутонијум, а због огромне отровности овог елемента данас су такви тестови забрањени.
–ß–∞–∫ –∏ –ø—Ä–µ –æ—Ç–∫—Ä–∏—õ–∞ –ø–ª—É—Ç–æ–Ω–∏—ò—É–º–∞, —É –ù–µ–º–∞—á–∫–æ—ò —ò–µ –ö–∞—Ä–ª –§—Ä–∏–¥—Ä–∏—Ö —Ñ–æ–Ω –í–∞—ò—Ü–µ–∫–µ—Ä –Ω–∞–≥–æ–≤–∏—ò–µ—Å—Ç–∏–æ –¥–∞ —ò–µ —É –Ω—É–∫–ª–µ–∞—Ä–Ω–∏–º —Ä–µ–∞–∫—Ç–æ—Ä–∏–º–∞ –º–æ–≥—É—õ –Ω–∞—Å—Ç–∞–Ω–∞–∫ –Ω–æ–≤–æ–≥ –µ–ª–µ–º–µ–Ω—Ç–∞ –µ–∫–∞- —Ä–µ–Ω–∏—ò—É–º–∞ (—Ç—ò. 239 Eka Re).[ 8] –§—Ä–∏–¥—Ä–∏—Ö –ì–µ–æ—Ä–≥ –•–æ—É—Ç–µ—Ä–º–∞–Ω—Å —ò–µ —Ç–∞–∫–æ—í–µ 1942. –ø—Ä–µ–¥–≤–∏–¥–µ–æ —Ç–µ–æ—Ä–µ—Ç—Å–∫–æ –ø–æ—Å—Ç–æ—ò–∞—ö–µ –Ω–µ–∫–æ–≥ —Ç—Ä–∞–Ω—Å—É—Ä–∞–Ω–∏—ò—É–º—Å–∫–æ–≥ –µ–ª–µ–º–µ–Ω—Ç–∞ —É —Å–≤–æ–º —Ç–∞—ò–Ω–æ–º –∏–∑–≤—ò–µ—à—Ç–∞—ò—É. –ú–µ—í—É—Ç–∏–º —É –æ–∫–≤–∏—Ä–∏–º–∞ –Ω–∞—Ü–∏—Å—Ç–∏—á–∫–æ–≥ —É—Ä–∞–Ω–∏—ò—É–º—Å–∫–æ–≥ –ø—Ä–æ—ò–µ–∫—Ç–∞, –ø—Ä–µ–º–∞ –¥–∞–Ω–∞—à—ö–∏–º —Å–∞–∑–Ω–∞—ö–∏–º–∞, –¥–æ –∫—Ä–∞—ò–∞ –î—Ä—É–≥–æ–≥ —Å–≤–µ—Ç—Å–∫–æ–≥ —Ä–∞—Ç–∞ –Ω–∏—ò–µ –¥–æ—à–ª–æ –¥–æ —Å–∏–Ω—Ç–µ–∑–µ –ø–ª—É—Ç–æ–Ω–∏—ò—É–º–∞.[ 9]
При нормалним условима температуре и притиска, плутонијум је сребрнасто-сјајни тешки метал, веома велике густине (19,86 g/cm3 ). Као и сви актиноиди, он такође постоји само у виду радиоактивних изотопа. Он се загрејава сам од себе, тако да на пример 100 грама плутонијума емитује око 0,2 вата топлоте (односи се на изотоп 239 Pu).[ 11] електричне струје . Метал се кристализује независно од температуре у укупно шест алотропских модификација . Оне се једним делом знатно разликују по својој густини. На собној температури стабилна модификација α-Pu је моноклинска . Код плутонијума при вишим температурама јавља се врло редак случај аномалије густине, јер она расте при преласку из δ' модификације у ε модификацију. При његовом топљењу, слично као код воде , густина му расте.[ 12] вискозност од свих елемената у течном стању.[ 13] магнетне сусцептибилности за метале и тенденције усмеравања при ниским температурама, плутонијум не показује усмеравање у широким распонима температуре па се стога може сматрати да је парамагнетичан.[ 12] 239 Pu. Из истог разлога немогуће је постићи температуре плутонијума блиске апсолутној нули.
–ú–æ–¥–∏—Ñ–∏–∫–∞—Ü–∏—ò–∞ –ø—Ä–∏ –∞—Ç–º–æ—Å—Ñ–µ—Ä—Å–∫–æ–º –ø—Ä–∏—Ç–∏—Å–∫—É
–û–ø–∏—Å
–°—Ç–∞–±–∏–ª–∞–Ω —É
–ì—É—Å—Ç–∏–Ω–∞ (—Ç–µ–º–ø–µ—Ä–∞—Ç—É—Ä–∞)
–ö—Ä–∏—Å—Ç–∞–ª–Ω–∏ —Å–∏—Å—Ç–µ–º
–ë—Ä–∞–≤–µ–æ–≤–∞ —Ä–µ—à–µ—Ç–∫–∞
–ü—Ä–æ—Å—Ç–æ—Ä–Ω–∞ –≥—Ä—É–ø–∞
α-Pu[ 14]
0 K – 395 K
19,77 g/cm³ (293 K)
–º–æ–Ω–æ–∫–ª–∏–Ω—Å–∫–∏
–ø—Ä–∏–º–∏—Ç–∏–≤–Ω–∞
P 21 /m (–±—Ä. 11)
β-Pu[ 15]
395 K – 479 K
17,7 g/cm³ (395 K)
–º–æ–Ω–æ–∫–ª–∏–Ω—Å–∫–∏
—Ü–µ–Ω—Ç—Ä–∏—Ä–∞–Ω–∞ –ø–æ –±–∞–∑–∏
I 2/m (–±—Ä. 12 –ø–æ–∑. 3)
γ-Pu[ 16]
479 K – 592 K
17,14 g/cm³ (479 K)
–æ—Ä—Ç–æ—Ä–æ–º–≥–∏—á–Ω–∏
–ø–ª–æ—à–Ω–æ —Ü–µ–Ω—Ç—Ä–∏—Ä–∞–Ω–∞
Fddd (–±—Ä. 70)
δ-Pu[ 17]
592 K – 730 K
15,9 g/cm³ (592 K)
–º–æ–Ω–æ–∫–ª–∏–Ω—Å–∫–∏
—Ü–µ–Ω—Ç—Ä–∏—Ä–∞–Ω–∞ –ø–æ –±–∞–∑–∏
Cm (–±—Ä. 8)
δ'-Pu[ 18]
730 K – 749 K
16,0 g/cm³ (730 K)
—Ç–µ—Ç—Ä–∞–≥–æ–Ω–∞–ª–Ω–∏
–ø—Ä–æ—Å—Ç–æ—Ä–Ω–æ —Ü–µ–Ω—Ç—Ä–∏—Ä–∞–Ω–∞
I 4/mmm (–±—Ä. 139)
ε-Pu[ 19]
749 K – 914 K
16,5 g/cm³ (749 K)
–∫—É–±–Ω–Ω–∏
–ø—Ä–æ—Å—Ç–æ—Ä–Ω–æ —Ü–µ–Ω—Ç—Ä–∏—Ä–∞–Ω–∞
Im
3
¯
{\displaystyle {\bar {3}}}
m
—Ç–µ—á–Ω–∏[ 20]
914 K – 3503 K
16,63 g/cm³ (914 K)
—
—
—
Осим наведених, познате су и модификације при високом притиску, које се добију из α-Pu при притиску изнад 40 GPa, а кристализирају се у просторној групи P 63 .[ 21]
–Ý–∞–∑–Ω–∞ –æ–∫—Å–∏–¥–∞—Ü–∏–æ–Ω–∞ —Å—Ç–∞—ö–∞ –ø–ª—É—Ç–æ–Ω–∏—ò—É–º–∞ —É –≤–æ–¥–µ–Ω–∏–º —Ä–∞—Å—Ç–≤–æ—Ä–∏–º–∞ –ü–ª—É—Ç–æ–Ω–∏—ò—É–º —ò–µ –Ω–µ–ø–ª–µ–º–µ–Ω–∏—Ç–∏, –≤–µ–æ–º–∞ —Ä–µ–∞–∫—Ç–∏–≤–Ω–∏ –º–µ—Ç–∞–ª . –ò–∑–ª–æ–∂–µ–Ω –≤–∞–∑–¥—É—Ö—É, –±—Ä–∑–æ —Ä–µ–∞–≥—É—ò–µ —Å –∫–∏—Å–µ–æ–Ω–∏–∫–æ–º –∏ –≤–ª–∞–≥–æ–º. –ü—Ä–∏ —Ç–æ–º–µ –º–µ—Ç–∞–ª –ø–æ—Å—Ç–∞—ò–µ –º–∞—Ç –∏ –ø—Ä–µ–≤–ª–∞—á–∏ —Å–µ —Ç–∞–º–Ω–∏–º, –ø–ª–∞–≤–æ-—Ü—Ä–Ω–∏–º —Å–ª–æ—ò–µ–º –æ–∫—Å–∏–¥–∞, –¥–æ–∫ –¥—É–∂–∏–º —Å—Ç–∞—ò–∞—ö–µ–º –Ω–∞ –≤–∞–∑–¥—É—Ö—É —Å—Ç–≤–∞—Ä–∞ —Å–µ —Ç–∞–º–Ω–∏—ò–∏, —Å–∏–≤–æ-–∑–µ–ª–µ–Ω–∏, –ø—Ä–∞—à–∫–∞—Å—Ç–∏ —Å–ª–æ—ò –æ–∫—Å–∏–¥–∞ –∫–æ—ò–∏ –ª–∞–∫–æ —Å–∫–∏–¥–∞.[ 22] –Ω–µ–º–µ—Ç–∞–ª–∞ –∏ –≤–æ–¥–æ–º. –ú–µ—í—É—Ç–∏–º –Ω–∞ —Å–æ–±–Ω–æ—ò —Ç–µ–º–ø–µ—Ä–∞—Ç—É—Ä–∏, –ø–ª—É—Ç–æ–Ω–∏—ò—É–º –Ω–µ –Ω–∞–ø–∞–¥–∞—ò—É –Ω–∏ –±–∞–∑–∏–Ω–∏ —Ä–∞—Å—Ç–≤–æ—Ä–∏, –Ω–∏—Ç–∏ –≤–æ–¥–∞ . –£ –∫–æ–Ω—Ü–µ–Ω—Ç—Ä–∏—Ä–∞–Ω–æ—ò –∞–∑–æ—Ç–Ω–æ—ò –∫–∏—Å–µ–ª–∏–Ω–∏ –æ–Ω –Ω–∏—ò–µ —Ä–∞—Å—Ç–≤–æ—Ä—ô–∏–≤ –∑–±–æ–≥ –ø–∞—Å–∏–≤–∏–∑–∞—Ü–∏—ò–µ —Å–≤–æ—ò–µ –ø–æ–≤—Ä—à–∏–Ω–µ.[ 11] —Ö–ª–æ—Ä–æ–≤–æ–¥–æ–Ω–∏—á–Ω–æ—ò –∏ –∞–∑–æ—Ç–Ω–æ—ò –∫–∏—Å–µ–ª–∏–Ω–∏ –∞–ª–∏ —É–∑ –¥–æ–¥–∞—Ç–∞–∫ —Ñ–ª—É–æ—Ä–∏–¥–∞. –£ —Ç–æ–º —Å–ª—É—á–∞—ò—É, —ò–æ–Ω–∏ —Ñ–ª—É–æ—Ä–∏–¥–∞ —Å–µ –ø–æ–Ω–∏—à—Ç–∞–≤–∞—ò—É –∏ –æ–Ω–µ–º–æ–≥—É—õ–∞–≤–∞—ò—É –ø–∞—Å–∏–≤–∏–∑–∏—Ä–∞—ö–µ –º–µ—Ç–∞–ª–∞ –∫–æ—ò–µ —Å–µ –∏–Ω–∞—á–µ —ò–∞–≤—ô–∞ –Ω–∞–ø–∞–¥–∞—ö–µ–º —á–∏—Å—Ç–µ –∞–∑–æ—Ç–Ω–µ –∫–∏—Å–µ–ª–∏–Ω–µ. –•–µ–º–∏—ò—Å–∫–µ –æ—Å–æ–±–∏–Ω–µ –ø–ª—É—Ç–æ–Ω–∏—ò—É–º–∞ —É–≥–ª–∞–≤–Ω–æ–º —Å—É —Å–ª–∏—á–Ω–µ –∫–∞–æ –∏ –∫–æ–¥ –æ—Å—Ç–∞–ª–∏—Ö –∞–∫—Ç–∏–Ω–æ–∏–¥–∞. –ö–∞–æ –∏ –∫–æ–¥ –≤–µ—õ–∏–Ω–µ –æ–≤–∏—Ö –µ–ª–µ–º–µ–Ω–∞—Ç–∞, —ö–µ–≥–æ–≤–µ —Ö–µ–º–∏—ò—Å–∫–µ –æ—Å–æ–±–∏–Ω–µ —Å—É –ø–æ–¥ –∑–Ω–∞—Ç–Ω–∏–º —É—Ç–∏—Ü–∞—ò–µ–º —ö–µ–≥–æ–≤–µ —Å–Ω–∞–∂–Ω–µ —Ä–∞–¥–∏–æ–∞–∫—Ç–∏–≤–Ω–æ—Å—Ç–∏, –∞ –∑–±–æ–≥ –∑–∞–≥—Ä–µ—ò–∞–≤–∞—ö–∞ –º–µ—Ç–∞–ª–∞ –∏ –µ–º–∏—Ç–æ–≤–∞—ö–∞ —ò–∞–∫–æ–≥ —Ä–∞–¥–∏–æ–∞–∫—Ç–∏–≤–Ω–æ–≥ –∑—Ä–∞—á–µ—ö–∞, —ö–µ–≥–æ–≤–µ –≤–µ–∑–µ —Å–∞ –¥—Ä—É–≥–∏–º –µ–ª–µ–º–µ–Ω—Ç–∏–º–∞ –≤—Ä–ª–æ –ª–∞–∫–æ –ø—É—Ü–∞—ò—É.
–û–≤–∞—ò –µ–ª–µ–º–µ–Ω—Ç –º–æ–∂–µ –¥–∞ –≥—Ä–∞–¥–∏ —Ü–µ–ª–∏ –Ω–∏–∑ —ò–µ–¥–∏—ö–µ—ö–∞ —É –∫–æ—ò–∏–º–∞ —Å–µ –º–æ–∂–µ –Ω–∞–ª–∞–∑–∏—Ç–∏ —É –æ–∫—Å–∏–¥–∞—Ü–∏–æ–Ω–∏–º —Å—Ç–∞—ö–∏–º–∞ –æ–¥ +3 –¥–æ +7, —à—Ç–æ –∑–Ω–∞—á–∏ –¥–∞ –ø–ª—É—Ç–æ–Ω–∏—ò—É–º –∑–∞—ò–µ–¥–Ω–æ —Å –Ω–µ–ø—Ç—É–Ω–∏—ò–µ–º –≥—Ä–∞–¥–∏ –Ω–∞—ò–≤–∏—à–∞ –æ–∫—Å–∏–¥–∞—Ü–∏–æ–Ω–∞ —Å—Ç–∞—ö–∞ –º–µ—í—É —Å–≤–∏–º –∞–∫—Ç–∏–Ω–æ–∏–¥–∏–º–∞. –ù–∞—ò—Å—Ç–∞–±–∏–ª–Ω–∏—ò–∏ —ò–µ —É –æ–∫—Å–∏–¥–∞—Ü–∏–æ–Ω–æ–º —Å—Ç–∞—ö—É +4. –£ –≤–æ–¥–µ–Ω–∏–º —Ä–∞—Å—Ç–≤–æ—Ä–∏–º–∞, —ò–æ–Ω–∏ –ø–ª—É—Ç–æ–Ω–∏—ò—É–º–∞ –∏–º–∞—ò—É –∫–∞—Ä–∞–∫—Ç–µ—Ä–∏—Å—Ç–∏—á–Ω–µ –±–æ—ò–µ. –¢–∞–∫–æ –Ω–∞ –ø—Ä–∏–º–µ—Ä —ò–æ–Ω Pu3+ —ò–µ —ô—É–±–∏—á–∞—Å—Ç, —ò–æ–Ω Pu4+ —Å–º–µ—í, PuV O2 + —Ä–æ–∑–µ –±–æ—ò–µ, PuVI O2 2+ –Ω–∞—Ä–∞–Ω—ü–∞—Å—Ç, –∞ PuVII O2 3+ –∑–µ–ª–µ–Ω.
До данас је измерено и испитано 20 изотопа и 15 нуклеарних изомера плутонијума, чији масени бројеви се крећу од 228 до 247.[ 24] Времена полураспада се крећу од 37 · 10−12 секунди за изомер 236m 1 Pu до око 80 милиона година за изотоп 244 Pu. „Најдуговјечнији” изотопи са временима полураспада дужим од 11 дана имају масене бројеве између 236 и 244. Једини изузетак међу њима је 243 Pu чије време полураспада износи краће од 5 сати.[ 24]
–ò–∑–æ—Ç–æ–ø 236 Pu—Ç–æ—Ä–∏—ò—É–º–æ–≤–æ–≥ –Ω–∏–∑–∞ . –û–Ω –∏–º–∞ –≤—Ä–µ–º–µ –ø–æ–ª—É—Ä–∞—Å–ø–∞–¥–∞ –æ–¥ 2,858 –≥–æ–¥–∏–Ω–µ,[ 24] 232 U, –∫–æ—ò–∏ —Å–µ –¥–∞—ô–µ —Å–∞ –≤—Ä–µ–º–µ–Ω–æ–º –ø–æ–ª—É—Ä–∞—Å–ø–∞–¥–∞ –æ–¥ 68,9 –≥–æ–¥–∏–Ω–∞ –æ–ø–µ—Ç —Ä–∞—Å–ø–∞–¥–∞ –Ω–∞ 228 Th, —à—Ç–æ –ø—Ä–µ–¥—Å—Ç–∞–≤—ô–∞ –≥–ª–∞–≤–Ω–∏ –Ω–∏–∑ —Ä–∞—Å–ø–∞–¥–∞. –û–≤–∞—ò –∏–∑–æ—Ç–æ–ø —Å–µ –¥–æ–±–∏—ò–∞ —É –≤–µ–æ–º–∞ –º–∞–ª–∏–º –∫–æ–ª–∏—á–∏–Ω–∞–º–∞ —É –Ω—É–∫–ª–µ–∞—Ä–Ω–∏–º —Ä–µ–∞–∫—Ç–æ—Ä–∏–º–∞ –∫–æ—ò–∏ —Ä–∞–¥–µ –Ω–∞ –±–∞–∑–∏ —É—Ä–∞–Ω–∏—ò—É–º–∞.
Изотоп 237 Puзахвата електрона током времена полураспада од 45,2 дана[ 24] нептунијума 237 Np са вероватноћом од 99,9958%, што представља главну полазну тачку нептунијумовог низа . Осталих 0,0042% атома овог изотопа распада се α-распадом до уранијума 233 U, који се такође распада нептунијумовим низом .
238 Pu[ 24] 234 U те се даље распада низом распада уранијум-радијумовим низом 239 Pu[ 24] 235 U. Даљи распад одвија се путем уранијум-актинијумовог низа , за природну радиоактивност, почев од изотопа 235 U. Само 3 · 10−10 % атома овог изотопа распада се спонтаним распадом .Изотоп 240 Pu[ 24] 236 U емитујући α-зрачење. Тај изотоп уранијума се распада с временом полураспада од 23,4 милиона година до природног изотопа торијума 232 Th. Даљи распад одвија се дуж торијумовог низа .
Изотоп 241 Puнептунијумовог низа , јер (при продужењу низа) се налази пре нептунијума. Он се распада са временом полураспада од 14,35 година[ 24] америцијума 241 Am, док се с вероватноћом од само 0,0025% распада α-распадом на уранијум 237 U. Даље се америцијум 241 Am α-распадом и уранијум237 U распадају до истог дугоживећег изотопа нептунијума 237 Np.
Плутонијум 242 Pu238 Pu. Међутим, док 238 Pu долази у низ распада као споредни ланац на 234 U, изотоп 242 Pu стоји још више пре уранијума 238 U. Плутонијум 242 Pu се распада α-распадом на 238 U, представљајући почетак природног уранијум-радијумовог низа. Са временом полураспада од 375 хиљада година,[ 24] 242 Pu је најдуговечнији изотоп плутонијума након 244 Pu.
243 Pu[ 24] 243 Am, који даље прелази у нептунијум 239 Np а овај даље се распада на плутонијум 239 Pu. На тај начин овај изотоп представља продужетак уранијум-актинијумовог низа.Изотоп плутонијума 244 Pu[ 25] [ 24] плутонијум-торијумов низ . Изотоп 244 Pu се распада α-распадом на 240 U, овај двоструким β-распадом преко нептунијума 240 Np до 240 Pu, а овај опет се путем даљњег двоструког α-распада преко 236 U до торијума 232 Th. Након изотопа торијума следи распад дуж торијумовог низа.
^ Meija, J.; et al. (2016). „Atomic weights of the elements 2013 (IUPAC Technical Report)” . Pure and Applied Chemistry 88 (3): 265—291. doi :10.1515/pac-2015-0305 . ^ Housecroft, C. E.; Sharpe, A. G. (2008). Inorganic Chemistry (3. изд.). Prentice Hall. ISBN 978-0-13-175553-6 . ^ Parkes, G.D. & Phil, D. (1973). Melorova moderna neorganska hemija . Beograd: Naučna knjiga. ^ G. T. Seaborg; E. McMillan; J. W. Kennedy; A. C. Wahl (1946). „Radioactive Element 94 from Deuterons on Uranium”. Physical Review . 69 (7–8): 366–367. doi :10.1103/PhysRev.69.367 . ^ J. W. Kennedy; G. T. Seaborg; E. Segrè; A. C. Wahl (1946). „Properties of Element 94”. Physical Review . 70 (7–8): 555—556. doi :10.1103/PhysRev.70.555 . ^ B. B. Cunningham; L. B. Werner (1949). „The First Isolation Of Plutonium”. Journal of the American Chemical Society . 71 (5): 1521—1528. doi :10.1021/ja01173a001 . ^ „Carl Friedrich von Weizsäcker: Eine Möglichkeit der Energiegewinnung aus Uran 238, 17. Juli 1940” . Geheimdokumente zum deutschen Atomprogramm 1938–1945 . Deutsches Museum. Приступљено 13. 12. 2016 . ^ Markus Becker (19. 3. 2009). „Nuklear-Forensik: "Heisenberg-Würfel" verrät Details über Hitlers Atomprogramm” . Spiegel Online . Приступљено 13. 12. 2016 . ^ а б Norman N. Greenwood; Alan Earnshaw (1988). Chemie der Elemente (1 изд.). Weinheim: VCH Verlagsgesellschaft. ISBN 3-527-26169-9 . ^ а б „Plutonium: An Element at odds with itself” (pdf) . Los Alamos Science. 2000. Приступљено 19. 10. 2017 . ^ „Plutonium – Element mit vielen Facetten” . kernchemie.de (на језику: немачки). Приступљено 19. 10. 2017 . ^ W. H. Zachariasen; F. H. Ellinger (1963). „The Crystal Structure of alpha Plutonium Metal”. Acta Cryst . 16 : 777—783. doi :10.1107/S0365110X63002012 . ^ W. H. Zachariasen; F. H. Ellinger (1963). „The Crystal Structure of beta Plutonium Metal”. Acta Cryst . 16 : 369—375. doi :10.1107/S0365110X63000992 . ^ W. H. Zachariasen (1955). „Crystal Chemical Studies of the 5f-Series of Elements. XXIV. The Crystal Structure and Thermal Expansion of γ-Plutonium”. Acta Cryst . 8 : 431—433. doi :10.1107/S0365110X55001357 . ^ K. T. Moore; P. Söderlind; A. J. Schwartz; D. E. Laughlin (2006). „Symmetry and Stability of δ Plutonium: The Influence of Electronic Structure”. Physical Review Letters . 96 (20): 206402/1—206402/4. doi :10.1103/PhysRevLett.96.206402 . ^ F. H. Ellinger: Crystal structure of delta' plutonium and the thermal expansion characteristics of delta, delta' and epsilon plutonium Journal of Metals. 8, 1956, str. 1256–1259.
^ J. B. Ball, J. A. Lee, P. G. Mardon, J. A. L. Robertson: Determination de quelques proprietes physiques du plutonium metal. u: Memoires Scientifiques de la Revue de Metallurgie. 57, 1960, str. 49–56.
^ David R. Lide, ур. (2009). „Magnetic Susceptibility of the Elements and Inorganic Compounds”. CRC Handbook of Chemistry and Physics ISBN 9781420090840 . ^ S. Dabos-Seignon; J. P. Dancausse; R. Gering; S. Heathman; U. Benedict (1993). „Pressure induced phase transition in α-Pu” . Journal of Alloys and Compounds . 190 : 237—242. doi :10.1016/0925-8388(93)90404-B . ^ Georg Brauer (1978). Handbuch der Präparativen Anorganischen Chemie . 2 (3 изд.). Stuttgart: Enke. стр. 1293. ISBN 3-432-87813-3 . ^ а б в г д ђ е ж з и ј G. Audi; O. Bersillon; J. Blachot; A. H. Wapstra (2003). „The NUBASE evaluation of nuclear and decay properties” (PDF) . 729 . Nuclear Physics A.: 105—110. doi :10.1016/S0375-9474(97)00482-X . Архивирано из оригинала (pdf) 20. 7. 2011. г. Приступљено 11. 2. 2017 . ^ D. C. Hoffman; F. O. Lawrence; J. L. Mewherter; F. M. Rourke (1971). „Detection of Plutonium-244 in Nature” . Nature . 234 : 132—134. doi :10.1038/234132a0 .
Asimov, Isaac (1988). „Nuclear Reactors”. Understanding Physics . New York: Barnes & Noble Publishing. ISBN 0-88029-251-2 . Bernstein, Jeremy (2007). Plutonium: a History of the World's most Dangerous Element ISBN 978-0-309-10296-4 . OCLC 76481517 . Clark, Ronald (1961). The Birth of the Bomb: The Untold Story of Britain's Part in the Weapon That Changed the World OCLC 824335 . Eagleson, Mary (1994). Concise Encyclopedia Chemistry ISBN 978-3-11-011451-5 . Emsley, John (2001). „Plutonium”. Nature's Building Blocks: An A–Z Guide to the Elements . Oxford (UK): Oxford University Press. ISBN 0-19-850340-7 . Gosling, F. G. (1999). The Manhattan Project: Making the Atomic Bomb (PDF) . Oak Ridge: United States Department of Energy. ISBN 0-7881-7880-6 . DOE/MA-0001-01/99. Архивирано из оригинала (PDF) 24. 2. 2009. г. Приступљено 15. 2. 2009 . Greenwood, N. N.; Earnshaw, A. (1997). Chemistry of the Elements (2nd изд.). Oxford (UK): Butterworth-Heinemann. ISBN 0-7506-3365-4 . Heiserman, David L. (1992). „Element 94: Plutonium”. Exploring Chemical Elements and their Compounds 337 –340. ISBN 0-8306-3018-X . Hoddeson, Lillian; Henriksen, Paul W.; Meade, Roger A.; Westfall, Catherine L. (1993). Critical Assembly: A Technical History of Los Alamos During the Oppenheimer Years, 1943–1945 ISBN 0-521-44132-3 . OCLC 26764320 . Hunner, Jon (2004). Inventing Los Alamos . ISBN 978-0-8061-3891-6 . Hurst, D. G.; Ward, A. G. (1956). Canadian Research Reactors (PDF) . Ottawa: Atomic Energy of Canada Limited. OCLC 719819357 . Приступљено 6. 2. 2015 . Jha, D. K. (2004). Nuclear Energy ISBN 81-7141-884-8 . Kaku, Michio; Trainer, Jennifer (1983). Nuclear Power, Both Sides: The Best Arguments for and Against the Most Controversial Technology ISBN 9780393301281 . Приступљено 8. 12. 2013 . Kay, A. E. (1965). plutonium 1965 Lide, David R., ур. (2006). Handbook of Chemistry and Physics (87th изд.). Boca Raton: CRC Press, Taylor & Francis Group. ISBN 0-8493-0487-3 . Magurno, B. A.; Pearlstein, S., ур. (1981). Proceedings of the conference on nuclear data evaluation methods and procedures. BNL-NCS 51363. (PDF) . II . Upton: Brookhaven National Laboratory . Приступљено 6. 8. 2014 . Martin, James E. (2000). Physics for Radiation Protection . Wiley-Interscience. ISBN 0-471-35373-6 . McLaughlin, Thomas P.; Monahan, Shean P.; Pruvost, Norman L. (2000). A Review of Criticality Accidents (PDF) . Los Alamos: Los Alamos National Laboratory. LA-13638. Архивирано из оригинала (PDF) 18. 01. 2017. г. Приступљено 6. 2. 2015 . Miner, William N.; Schonfeld, Fred W. (1968). „Plutonium”. Ур.: Clifford A. Hampel. The Encyclopedia of the Chemical Elements 540 –546. LCCN 68029938 . Moody, Kenton James; Hutcheon, Ian D.; Grant, Patrick M. (2005). Nuclear forensic analysis ISBN 0-8493-1513-1 . Rhodes, Richard (1986). The Making of the Atomic Bomb ISBN 0-671-65719-4 . Seaborg, G. T.; Seaborg, E. (2001). Adventures in the Atomic Age: From Watts to Washington ISBN 0-374-29991-9 . Sklar, Morty (1984). Nuke-Rebuke: Writers & Artists Against Nuclear Energy & Weapons . The Contemporary anthology series. The Spirit That Moves Us Press. Stockholm International Peace Research Institute (2007). SIPRI Yearbook 2007: Armaments, Disarmament, and International Security ISBN 978-0-19-923021-1 . Till, C. E.; Chang, Y. I. (2011). Plentiful Energy: The Story of the Integral Fast Reactor, the Complex History of a Simple Reactor Technology, with Emphasis on Its Scientific Basis for Non-specialists ISBN 978-1-4663-8460-6 . Wahlen, R. K. (1989). History of 100-B Area (PDF) . Richland, Washington: Westinghouse Hanford Company. WHC-EP-0273. Архивирано из оригинала (PDF) 27. 3. 2009. г. Приступљено 15. 2. 2009 . Welsome, Eileen (2000). The Plutonium Files: America's Secret Medical Experiments in the Cold War . New York: Random House. ISBN 0-385-31954-1 .
„Alsos Digital Library for Nuclear Issues - Plutonium” . Washington and Lee University . Архивирано из оригинала 3. 2. 2009. г. Приступљено 15. 2. 2009 . Sutcliffe, W. G.; et al. (1995). „A Perspective on the Dangers of Plutonium” . Lawrence Livermore National Laboratory . Архивирано из оригинала 29. 9. 2006. г. Johnson, C. M.; Davis, Z.S. (1997). „Nuclear Weapons: Disposal Options for Surplus Weapons-Usable Plutonium” . CRS Report for Congress # 97-564 ENR . Приступљено 15. 2. 2009 . „Physical, Nuclear, and Chemical, Properties of Plutonium” . IEER . 2005. Приступљено 15. 2. 2009 . Bhadeshia, H. „Plutonium crystallography” . Samuels, D. (2005). „End of the Plutonium Age” . Discover Magazine . 26 (11). Pike, J.; Sherman, R. (2000). „Plutonium production” . Federation of American Scientists . Архивирано из оригинала 3. 2. 2009. г. Приступљено 15. 2. 2009 . „Plutonium Manufacture and Fabrication” . Ong, C. (1999). „World Plutonium Inventories” . Nuclear Files.org. Архивирано из оригинала 5. 8. 2014. г. Приступљено 15. 2. 2009 . „Challenges in Plutonium Science” . Los Alamos Science . I & II (26). 2000. Приступљено 15. 2. 2009 . „Plutonium” . Royal Society of Chemistry . Приступљено 6. 2. 2015 . „Plutonium” . The Periodic Table of Videos . University of Nottingham. Приступљено 6. 2. 2015 .
–ú–µ—Å—Ç–∞ –ê–¥–º–∏–Ω–∏—Å—Ç—Ä–∞—Ç–æ—Ä–∏ –ù–∞—É—á–Ω–∏—Ü–∏ –û–ø–µ—Ä–∞—Ü–∏—ò–µ –û—Ä—É–∂—ò–µ –ü–æ–≤–µ–∑–∞–Ω–µ —Ç–µ–º–µ
–î—Ä–∂–∞–≤–Ω–µ –û—Å—Ç–∞–ª–µ





![{\displaystyle \mathrm {^{238}_{\ 92}U\ +\ _{1}^{2}D\ \longrightarrow \ _{\ 93}^{238}Np\ +\ 2\ _{0}^{1}n\quad ;\quad _{\ 93}^{238}Np\ {\xrightarrow[{2,117\ d}]{\beta ^{-}}}\ _{\ 94}^{238}Pu} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/e1cea0855d09c23ed65d8571e341ca5b6e018ea6)
![{\displaystyle \mathrm {^{238}_{\ 92}U\ +\ _{0}^{1}n\ \longrightarrow \ _{\ 92}^{239}U\ {\xrightarrow[{23,5\ min}]{\beta ^{-}}}\ _{\ 93}^{239}Np\ {\xrightarrow[{2,3565\ d}]{\beta ^{-}}}\ _{\ 94}^{239}Pu} }](https://wikimedia.org/api/rest_v1/media/math/render/svg/12492af52719f167cf2db01c018abf105d690225)















