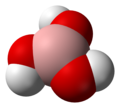
Борна киселина
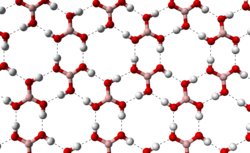
Борна киселина или ортоборна киселина — соединение од бор, кислород и водород со формула B(OH) Боринската киселина често се користи како антисептик, инсектицид, отпорник на пламен, апсорбер на неутрони или претходник на други соединенија на бор. Терминот „борна киселина“ исто така се користи генерички за која било оксокиселина на бор, како што е метаборната киселина HBO ИсторијаОртоборната киселина првпат била подготвена од Вилхелм Хомберг (1652-1715) од борат, со дејство на неоргански киселини, и го добила името sal sedativum Hombergi ("седативна сол на Хомберг"). Сепак, борната киселина и боратите се користеле уште од времето на старите Грци за чистење, зачувување храна и други активности.[1] Молекуларна и кристална структураТрите атоми на кислород формираат тригонална рамна геометрија околу борот. Должината на BO е 136 pm, а OH е 97 pm. Групата на молекуларна точка е C3h [2] Познати се две кристални форми на ортоборна киселина: триклинска и шестаголна. Првиот е најчест; вториот, кој е малку постабилен термодинамички, може да се добие со посебен метод на подготовка.[3] ТриклиникТриклинската форма на борна киселина се состои од слоеви наB(OH)
ПодготовкаБорна киселина може да се подготви со реакција на борат (натриум тетраборат декахидрат) со неорганска киселина, како што е хлороводородна киселина:
Исто така, се формира како нус-производ на хидролиза на трихалиди на бор и диборан:[5]
РеакцииПиролизаКога се загрева, ортоборната киселина се подложува на тристепена дехидрација. Пријавените преодни температури значително се разликуваат од извор до извор. Кога се загрева над 140 °C, ортоборната киселина дава метаборна киселина (HBO
Загревање на метаборна киселина над околу 180 °C елиминира друга молекула на вода која формира тетраборна киселина, исто така наречена пироборна киселина (H
Дополнително загревање (до околу 530 °C) доведува до бор триоксид:[6][7][8]
Воден растворКога ортоборната киселина се раствора во вода, таа делумно се дисоцира и дава метаборна киселина:
Растворот е благо кисел поради јонизација на киселините:
Сепак, Рамановата спектроскопијата на силно алкални раствори покажала присуство на тетрахидроксиборат јони,[9] и наведува некои да заклучат дека киселоста се должи исклучиво на апстракцијата на OH−
Еквивалентно,
Или, поточно,
Оваа реакција се јавува во два чекори, со неутрален комплекс акватрихидроксибор B(OH)
Оваа реакција може да се одликува како Луисова киселост на бор кон [HO]− Борна киселина, измешана со борат Na Раствор на сулфурна киселинаБорна киселина исто така се раствора во безводна сулфурна киселина според равенката [4]
ЕстерификацијаБорна киселина реагира со алкохоли за да формира боратни естри, B(OR)
Со вицинални диолиКиселоста на растворите на борна киселина е значително зголемена во присуство на цис - вицинални диоли (органски соединенија кои содржат слично ориентирани хидроксилни групи во соседните јаглеродни атоми,(R Тетрахидроксиборатниот анјон формиран при растворање спонтано реагира со овие диоли за да формира релативно стабилни анјонски естри кои содржат еден или два петчлени–B–O–C–C–O– прстени. На пример, реакцијата со манитол H(HCOH)
Давање на целокупната реакција
Стабилноста на овие естерски анјони на манитоборат ја поместува рамнотежата на десната страна и на тој начин ја зголемува киселоста на растворот за 5 реда на големина во споредба со онаа на чист борен оксид, намалувајќи го p K a од 9 на под 4 за доволна концентрација на манитол.[4][16] Добиениот раствор е наречен манитоборна киселина. Додавањето на манитол во првично неутрален раствор кој содржи борна киселина или едноставни борати ја намалува неговата pH доволно за да може да се титрира со силна база како NaOH, вклучително и со автоматизиран потенциометриски титратор. Ова својство се користи во аналитичката хемија за да се одреди содржината на борати во водените раствори, на пример за следење на исцрпувањето на борната киселина од неутроните во водата од примарното коло на реакторот светлина-вода кога соединението се додава како неутронски отров за време на полнење гориво. операции.[4] ТоксикологијаВрз основа на рејтингот на средна смртоносна доза кај цицачите (LD 50) од 2.660 mg/kg телесна маса, борната киселина е отровна само ако се зема внатрешно или се вдишува во големи количини. Четиринаесеттото издание на Мерк индексот покажува дека LD 50 на борната киселина е 5,14 g/kg за орални дози дадени на стаорци, и тоа од 5 до 20 g/kg предизвика смрт кај возрасни луѓе. За 70 кг возрасен, на долната граница од 5 g, 350 g може да предизвика смрт кај луѓето. За споредба, LD 50 на солта е пријавена дека е 3,75 g/kg кај стаорци според Мерковиот индекс. Според Агенцијата за токсични материи и регистар на болести, „Минималната смртоносна доза на проголтан бор (како борна киселина) беше пријавена дека е 2–3 g кај доенчиња, 5-6 g кај деца и 15-20 g кај возрасни. [. . . ] Сепак, преглед на 784 човечки труења со борна киселина (10-88 g) не објави смртни случаи, при што 88% од случаите се асимптоматски.“ [17] Долготрајната изложеност на борна киселина може да биде позагрижувачка, предизвикувајќи оштетување на бубрезите и евентуално откажување на бубрезите (видете ги врските подолу). Иако се чини дека не е канцероген, студиите кај кучиња пријавиле атрофија на тестисите по изложување на 32 mg/kg телесна тежина/ден во тек на 90 дена. Ова ниво, кога би било применливо за луѓе во иста доза, би било еднакво на кумулативна доза од 202 g во текот на 90 дена за 70 kg возрасен, не многу понизок од горенаведениот LD50 .[18] Според извештајот на CLH за борна киселина објавен од Бирото за хемиски супстанции во Лоѓ, Полска, борната киселина во високи дози покажува значителна развојна токсичност и тератогеност кај фетусите на зајаци, стаорци и глувци, како и кардиоваскуларни дефекти, скелетни варијации и благи бубрези лезии.[19] Како последица на 30-тата АТП на директивата на ЕУ 67/548/ЕЕЗ од август 2008 година, Европската комисија одлучила да ја измени својата класификација како репротоксична категорија 2 и да ги примени фразите за ризик R60 (може да ја наруши плодноста) и R61 (може да предизвика штета на нероденото дете).[20][21][22][23] На состанокот на Европската асоцијација за производство на дијагностика (EDMA) во 2010 година, биле дискутирани неколку нови дополнувања на списокот на кандидати за Супстанција со многу висока загриженост (SVHC) во однос на Регулативата за регистрација, евалуација, овластување и ограничување на хемикалиите од 2007 година (REACH). По регистрацијата и прегледот завршени како дел од REACH, класификацијата на борна киселина CAS 10043-35-3 / 11113-50-1 е наведена од 1 декември 2010 година е H360FD (може да ја оштети плодноста. Може да го оштети нероденото дете.) [24][25] УпотребаИндустријаПримарната индустриска употреба на борната киселина е во производството на монофиламентни фиберглас кои обично се нарекува текстилен фиберглас. Текстилниот фиберглас се користи за зајакнување на пластиката во апликации кои се движат од чамци, до индустриски цевки до компјутерски кола.[26] Во индустријата за накит, борната киселина често се користи во комбинација со денатуриран алкохол за да се намали површинската оксидација и на тој начин формирање на огнот на металите за време на операциите на жарење и лемење. Борната киселина се користи во производството на стакло во LCD рамни екрани. Во галванизацијата, борната киселина се користи како дел од некои сопственички формули. Една таква позната формула бара околу 1 до 10 однос на H3BO3 до Никл(II)-сулфат, многу мал дел од натриум лаурил сулфат и мал дел од H2SO4. Растворот на ортоборна киселина и борат во сооднос 4:5 се користи како средство за забавување на пожарот на дрво со импрегнација.[27] Исто така се користи во производството на забивачка маса, фин прав што содржи силициум диоксид кој се користи за производство на облоги на индукционите печки и керамика. Борна киселина се додава во борат за употреба како флукс за заварување од страна на ковачите.[28] Борна киселина, во комбинација со поливинил алкохол (PVA) или силиконско масло, се користи за производство на Silly Putty.[29] Борна киселина е присутна и во списокот на хемиски адитиви кои се користат за хидраулично фрактурирање (фрактура).[30] Често се користи заедно со гуарната гума како средство за вкрстено поврзување и желатинирање за контролирање на вискозноста и реологијата на течноста за фракинг инјектирана под висок притисок во бунарот. Важно е да се контролира вискозноста на течноста за да се држат во суспензија на долги транспортни растојанија зрната на средствата за потпора насочени кон одржување на пукнатините во шкрилците доволно отворени за да се олесни извлекувањето на гасот откако ќе се намали хидрауличниот притисок.[31][32][33] Реолошките својства на хидрогелот со вкрстено поврзана гуарска гума со бора главно зависат од pH вредноста.[34] Боринската киселина се користи во некои електрични осигурувачи од типот на исфрлање како средство за дејонизација/гаснење.[35] За време на електричен дефект во осигурувачот од типот на исфрлање, се создава плазма лак со распаѓање и брзо раздвојување со пружина на топливиот елемент, што е типично специјализирана метална прачка која минува низ компримирана маса на борна киселина во склопот на осигурувачите. Високотемпературната плазма предизвикува борната киселина брзо да се распаѓа на водена пареа и борен анхидрид, а производите на испарување пак ја дејонизираат плазмата, помагајќи да се прекине електричната грешка.[36] МедицинаБоринската киселина може да се користи како антисептик за помали изгореници или исекотини и понекогаш се користи во салфетки и облоги, како што е борната влакненца. Борна киселина се нанесува во многу разреден раствор како миење очи. Разредената борна киселина може да се користи како вагинален туш за лекување на бактериска вагиноза поради прекумерна алкалност,[37] како и кандидијаза поради не-албиканска кандида.[38] Борната киселина во голема мера ги поштедува лактобацилите во вагината.[39] Како TOL-463, тој е во развој како интравагинален лек за третман на бактериска вагиноза и вулвовагинална кандидијаза.[40][41][42] Како антибактериско соединение, борната киселина може да се користи и како третман на акни. Се користи и како превенција од спортско стапало, со ставање пудра во чорапите. Различни препарати може да се користат за лекување на некои видови на otitis externa (инфекција на увото) и кај луѓето и кај животните.[43] Конзервансот во шишињата со примероци од урина во Обединетото Кралство е борна киселина.[44] Растворите на борна киселина што се користат како миење очи или на абрадирана кожа се познати како токсични, особено за доенчињата, особено по повторна употреба; ова е поради неговата бавна стапка на елиминација.[45] Борната киселина е една од најчесто користените супстанции што може да се спротивстави на штетните ефекти на реактивната флуороводородна киселина (HF) по случаен контакт со кожата. Работи со присилување на слободното F− ИнсектицидиБоринската киселина за прв пат била регистрирана во САД како инсектицид во 1948 година за контрола на лебарки, термити, огнени мравки, болви, сребрени риби и многу други инсекти. Производот генерално се смета за безбеден за употреба во кујните за домаќинство за контрола на лебарки и мравки. Дејствува како стомачен отров што влијае на метаболизмот на инсектите, а сувиот прав е абразивен за егзоскелетите на инсектите.[47][48][49] Боринската киселина, исто така, има репутација како „подарок кој продолжува да убива“ со тоа што бубашвабите кои поминуваат низ областите со лесно прашина не умираат веднаш, туку дека ефектот е како парчиња стакло што ги сечат. Ова често му дозволува да се врати во гнездото каде што наскоро умира. Лебарките, бидејќи се канибалисти, јадат други убиени со контакт или консумирање на борна киселина, консумирајќи го прашокот заробен во мртвата лебарк и убивајќи ги исто така. ЗачувувањеВо комбинација со неговата употреба како инсектицид, борната киселина го спречува и уништува постоечкото влажно и суво гниење на дрвата. Може да се користи во комбинација со носач на етилен гликол за третирање на надворешното дрво против напад на габи и инсекти. Можно е да се купат шипки импрегнирани со борати за вметнување во дрво преку дупки за дупчење каде што се знае дека влагата и влагата се собираат и седат. Достапен е во форма на гел и форма на паста за инјектирање за третирање на дрво погодено од гниење без потреба од замена на дрвото. Концентратите на третмани базирани на борати може да се користат за да се спречи растот на лигите, мицелиумот и алгите, дури и во морските средини. Борната киселина се додава во солта за лекување на говеда, теле и овчи кожи. Ова помага да се контролира развојот на бактериите и помага да се контролираат инсектите. pH пуфер  Борната киселина во рамнотежа со својата конјугирана база широко се користи борат јонот (во опсегот на концентрација 50-100 ppm еквиваленти на бор) како примарен или дополнителен pH пуфер систем во базените. Борната киселина е слаба киселина, со p Ka (pH во која пуферирањето е најсилно бидејќи слободната киселина и борат јон се во еднакви концентрации) од 9,24 во чиста вода на 25 °C. Но, очигледниот p Ka е значително a во водите на базените или океаните поради интеракциите со разни други молекули во растворот. Ќе биде околу 9,0 во базен со солена вода. Без разлика која форма на растворлив бор е додадена, во рамките на прифатливиот опсег на pH и концентрација на бор за базени, борната киселина е доминантна форма во воден раствор, како што е прикажано на придружната слика. Системот борна киселина-борат може да биде корисен како примарен тампон систем (замена за бикарбонатниот систем со p Ka a1 = 6,0 и p K a2 = 9,4 при типични услови на базен со солена вода) во базени со генератори на хлор со солена вода кои имаат тенденција да покажат нагорно поместување на pH од работен опсег од pH 7,5–8,2. Капацитетот на пуферот е поголем против зголемувањето на pH (кон pKa околу 9,0), како што е илустрирано на придружниот график. Употребата на борна киселина во овој опсег на концентрации не дозволува какво било намалување на концентрацијата на слободната HOCl потребна за санитација на базенот, но може малку да додаде на фото-заштитните ефекти на цијануричната киселина и да даде други придобивки преку антикорозивна активност или согледана мекост на водата., во зависност од целокупниот состав на растворената супстанца во базенот.[50] ЛубрикантКолоидните суспензии на наночестички борна киселина растворени во нафта или растително масло можат да формираат извонреден лубрикант на керамички или метални површини [51] со коефициент на триење на лизгање што се намалува со зголемување на притисокот до вредност во опсег од 0,10 до 0,02. B(OH) Борната киселина се користи за подмачкување на таблите од каром и новоус, што овозможува побрза игра.[52] Јадрена енергијаБоринската киселина се користи во некои атомски централи како неутронски отров. Борот во борната киселина ја намалува веројатноста за топлинско цепење со апсорпција на некои топлински неутрони. Синџирните реакции на цепење генерално се водени од веројатноста слободните неутрони да резултираат со цепење и се одредуваат од материјалните и геометриските својства на реакторот. Природниот бор се состои од приближно 20% изотопи бор-10 и 80% бор-11. Борот-10 има висок пресек за апсорпција на нискоенергетски (топлински) неутрони. Со зголемување на концентрацијата на борна киселина во течноста за ладење на реакторот, веројатноста дека неутронот ќе предизвика цепење се намалува. Промените во концентрацијата на борната киселина можат ефикасно да ја регулираат стапката на цепење што се случува во реакторот. Борна киселина се користи само во реактори за вода под притисок (PWR), додека реакторите за врела вода (BWR) користат шема на контролна шипка и проток на течноста за ладење за контрола на моќноста. BWR користат воден раствор на борна киселина и борат или натриум пентаборат за систем за итно исклучување. Борна киселина може да се раствори во базени за потрошено гориво што се користат за складирање на елементите на потрошеното гориво . Концентрацијата е доволно висока за да се одржи множењето на неутроните на минимум. Борна киселина била фрлена над реакторот 4 на атомската централа Чернобил по неговото топење за да се спречи појава на друга реакција. ПиротехникаБорот се користи во пиротехниката за да се спречи реакцијата на формирање на амид помеѓу алуминиум и нитрати. Мала количина на борна киселина се додава во составот за да се неутрализираат алкалните амиди кои можат да реагираат со алуминиумот. Боринската киселина може да се користи како боја за да се направи огнот зелен. На пример, кога се раствора во метанол, популарно се користи од жонглери и огнени вртења за да се создаде длабок зелен пламен многу посилен од бакар сулфат.[53] ЗемјоделствоБорна киселина се користи за лекување или спречување на недостаток на бор во растенијата. Се користи и за зачувување на житарки како ориз и пченица.[54] Дополнителна литература
Наводи
Надворешни врски
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Portal di Ensiklopedia Dunia