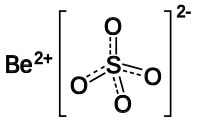
பெரிலியம் சல்பேட்டு
பெரிலியம் சல்பேட்டு (Beryllium sulfate) என்பது பொதுவாக நான்கு நீரேற்றாகவே காணப்படுகிறது எனவே இதனுடைய மூலக்கூற்று வாய்ப்பாடு BeSO4•4H2O என்றே எழுதப்படுகிறது. முதன்முதலில் 1815 ஆம் ஆண்டில் யோன்சு யோக்காப் பெர்சிலியசு பெரிலியம் சல்பேட்டைத் தனிமைப்படுத்தினார்.[3] பெரிலியம் உப்பின் நீர்க்கரைசலுடன் கந்தக அமிலம் சேர்த்து தொடர்ந்து ஆவியாக்கி படிகமாக்குவதன் மூலம் பெரிலியம் சல்பேட்டைத் தயாரிக்கலாம். நீரேற்று வடிவ பெரிலியம் சல்பேட்டை 400 0 செல்சியசு வெப்பநிலைக்கு சூடாக்குவதன் மூலம் நீரிலி உப்பைத் தயாரிக்க முடியும்[4]. இந்நான்கு நீரேற்றில் நான்முக Be(OH2)42+ அலகுகள் மற்றும் சல்பேட்டு எதிர்மின் அயனிகள் காணப்படுகின்றன. Be2+ [[அயனி|நேர்மின் அயனிகளின்] சிறிய அளவானது ஒருங்கிணைப்புக்குத் தேவையான நீர் மூலக்கூறுகளின் எண்ணிக்கையை உறுதிப்படுத்துகிறது. இதனை ஒத்த வரிசைச் சேர்மமான எண்முக Mg(OH2)62+ அலகுகள் கொண்ட மக்னீசியம் உப்பிலிருந்து பெரிலியம் சல்பேட்டு மாறுபடுகிறது.[5] பெரிலியம் சல்பேட்டின் நீரிலி வடிவச் சேர்மம் பெர்லினைட்டு கனிமத்தின் படிக அமைப்பை ஒத்துள்ளது. இவ்வமைப்பில் ஒன்றுவிட்டு ஒன்றாக Be மற்றும் S அணுக்கள் நான்முக ஒருங்கிணைப்பு முறைமையிலும் ஒவ்வொரு ஆக்சிசனும் இரண்டு (Be-O-S) ஒருங்கிணைப்புகளையும் கொண்டிருக்கின்றன. Be-O பிணைப்புகளுக்கு இடையிலான பிணைப்பு நீளம் 156 பைகோ மீட்டர்களாகவும் S-O பிணைப்புகளின் பிணைப்பு நீளம் 150 பைகோ மீட்டர்களாகவும் உள்ளது.[6] அணுக்கரு பிளவு கண்டறியப்பட்டதில் பெரிலியம் சல்பேட்டு மற்றும் ரேடியம் சல்பேட்டுகளின் கலவை நியூட்ரான் மூலமாகப் பயன்படுத்தப்பட்டது. மேற்கோள்கள்
வெளி இணைப்புகள் |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Portal di Ensiklopedia Dunia