Я«фЯ»єЯ«░Я«┐Я«▓Я«┐Я«»Я««Я»Ї Я«ЋЯ»ЂЯ«│Я»ІЯ«░Я»ѕЯ«ЪЯ»Ђ
Я«фЯ»єЯ«░Я«┐Я«▓Я«┐Я«»Я««Я»Ї Я«ЋЯ»ЂЯ«│Я»ІЯ«░Я»ѕЯ«ЪЯ»Ђ (Beryllium chloride) Я«јЯ«ЕЯ»ЇЯ«фЯ«цЯ»Ђ Я«фЯ»єЯ«░Я«┐Я«▓Я«┐Я«»Я««Я»Ї Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї Я«ЋЯ»ЂЯ«│Я»ІЯ«░Я«┐Я«ЕЯ»Ї Я«ЄЯ«БЯ»ѕЯ«еЯ»ЇЯ«цЯ»Ђ Я«ЅЯ«░Я»ЂЯ«хЯ«ЙЯ«ЋЯ»ЂЯ««Я»Ї Я«њЯ«░Я»Ђ Я«хЯ»ЄЯ«цЯ«┐Я«џЯ»Ї Я«џЯ»ЄЯ«░Я»ЇЯ««Я««Я«ЙЯ«ЋЯ»ЂЯ««Я»Ї. Я«ЄЯ«цЯ«ЕЯ»Ї Я««Я»ѓЯ«▓Я«ЋЯ»ЇЯ«ЋЯ»ѓЯ«▒Я»ЇЯ«▒Я»Ђ Я«хЯ«ЙЯ«»Я»ЇЯ«фЯ«ЙЯ«ЪЯ»Ђ BeCl2 Я«єЯ«ЋЯ»ЂЯ««Я»Ї Я«еЯ«┐Я«▒Я««Я«▒Я»ЇЯ«▒ Я«еЯ«┐Я«▓Я»ѕЯ«»Я«┐Я«▓Я»Ї Я«еЯ»ђЯ«░Я»ѕ Я«ЅЯ«▒Я«┐Я«ъЯ»ЇЯ«џЯ»ЂЯ««Я»Ї Я«цЯ«ЕЯ»ЇЯ««Я»ѕ Я«ЋЯ»іЯ«БЯ»ЇЯ«Ъ Я«цЯ«┐Я«БЯ»ЇЯ««Я««Я«ЙЯ«ЋЯ«ЋЯ»Ї Я«ЋЯ«ЙЯ«БЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЂЯ««Я»Ї Я«ЄЯ«џЯ»ЇЯ«џЯ»ЄЯ«░Я»ЇЯ««Я««Я»Ї Я««Я»ЂЯ«ЕЯ»ѕЯ«хЯ»ЂЯ«ЋЯ»Ї Я«ЋЯ«░Я»ѕЯ«фЯ»ЇЯ«фЯ«ЙЯ«ЕЯ»ЇЯ«ЋЯ«│Я»Ї Я«фЯ«▓Я«хЯ«▒Я»ЇЯ«▒Я«┐Я«▓Я»ЂЯ««Я»Ї Я«ЋЯ«░Я»ѕЯ«ЋЯ«┐Я«▒Я«цЯ»Ђ. Я«фЯ»єЯ«░Я«┐Я«▓Я«┐Я«»Я««Я»Ї Я«ЁЯ«▓Я»ЂЯ««Я«┐Я«ЕЯ«┐Я«»Я«цЯ»ЇЯ«цЯ»ЂЯ«ЪЯ«ЕЯ»Ї Я««Я»ѓЯ«▓Я»ѕЯ«хЯ«┐Я«ЪЯ»ЇЯ«ЪЯ«цЯ»Ї Я«цЯ»іЯ«ЪЯ«░Я»ЇЯ«фЯ»Ђ Я«ЋЯ»іЯ«БЯ»ЇЯ«ЪЯ«┐Я«░Я»ЂЯ«фЯ»ЇЯ«фЯ«цЯ«ЙЯ«▓Я»Ї Я«ЁЯ«▓Я»ЂЯ««Я«┐Я«ЕЯ«┐Я«»Я««Я»Ї Я«ЋЯ»ЂЯ«│Я»ІЯ«░Я»ѕЯ«ЪЯ«┐Я«ЕЯ»Ї Я«фЯ«БЯ»ЇЯ«фЯ»ЂЯ»ЇЯ«ЋЯ«│Я»ЂЯ«ЪЯ«ЕЯ»Ї Я«фЯ»єЯ«░Я»ЂЯ««Я«│Я«хЯ»Ђ Я«њЯ«цЯ»ЇЯ«цЯ«┐Я«░Я»ЂЯ«ЋЯ»ЇЯ«ЋЯ«┐Я«▒Я«цЯ»Ђ. Я«ЋЯ«ЪЯ»ЇЯ«ЪЯ««Я»ѕЯ«фЯ»ЇЯ«фЯ»ЂЯ««Я»Ї Я«цЯ»іЯ«ЋЯ»ЂЯ«цЯ»ЇЯ«цЯ«▓Я»ЂЯ««Я»ЇЯ«ЅЯ«»Я«░Я»Ї Я«хЯ»єЯ«фЯ»ЇЯ«фЯ«еЯ«┐Я«▓Я»ѕЯ«»Я«┐Я«▓Я»Ї Я«фЯ»єЯ«░Я«┐Я«▓Я«┐Я«»Я««Я»Ї Я«ЋЯ»ЂЯ«│Я»ІЯ«░Я«┐Я«ЕЯ»ЂЯ«ЪЯ«ЕЯ»Ї Я«хЯ«┐Я«ЕЯ»ѕЯ«фЯ»ЂЯ«░Я«┐Я«еЯ»ЇЯ«цЯ»Ђ Я«фЯ»єЯ«░Я«┐Я«▓Я«┐Я«»Я««Я»Ї Я«ЋЯ»ЂЯ«│Я»ІЯ«░Я»ѕЯ«ЪЯ»Ђ Я«цЯ«»Я«ЙЯ«░Я«┐Я«ЋЯ»ЇЯ«ЋЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЂЯ«ЋЯ«┐Я«▒Я«цЯ»Ђ:[1]. .
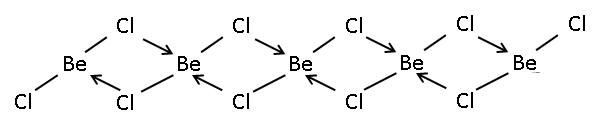
Я«фЯ»єЯ«░Я«┐Я«▓Я«┐Я«»Я««Я»Ї Я«єЯ«ЋЯ»ЇЯ«џЯ»ѕЯ«ЪЯ»ѕ Я«ЋЯ»ЂЯ«│Я»ІЯ«░Я«┐Я«ЕЯ»Ї Я««Я»ЂЯ«ЕЯ»ЇЯ«ЕЯ«┐Я«▓Я»ѕЯ«»Я«┐Я«▓Я»Ї[2] Я«хЯ»єЯ«фЯ»ЇЯ«фЯ««Я»ЇЯ«џЯ«ЙЯ«░Я»Ї Я«ЋЯ«ЙЯ«░Я»ЇЯ«фЯ«ЕЯ»Ї Я«њЯ«ЪЯ»ЂЯ«ЋЯ»ЇЯ«ЋЯ««Я»Ї Я«џЯ»єЯ«»Я»ЇЯ«цЯ»ЂЯ««Я»Ї, Я«фЯ»єЯ«░Я«┐Я«▓Я«┐Я«»Я«цЯ»ЇЯ«цЯ»ѕ Я«љЯ«цЯ«░Я«џЯ«ЕЯ»Ї Я«ЋЯ»ЂЯ«│Я»ІЯ«░Я»ѕЯ«ЪЯ»ЂЯ«ЪЯ«ЕЯ»Ї Я«џЯ»ЄЯ«░Я»ЇЯ«цЯ»ЇЯ«цЯ»Ђ Я«хЯ«┐Я«ЕЯ»ѕЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЂЯ«цЯ»ЇЯ«цЯ«┐Я«»Я»ЂЯ««Я»Ї Я«ЋЯ»ѓЯ«Ъ Я«фЯ»єЯ«░Я«┐Я«▓Я«┐Я«»Я««Я»Ї Я«ЋЯ»ЂЯ«│Я»ІЯ«░Я»ѕЯ«ЪЯ»ѕЯ«цЯ»Ї Я«цЯ«»Я«ЙЯ«░Я«┐Я«ЋЯ»ЇЯ«Ћ Я«ЄЯ«»Я«▓Я»ЂЯ««Я»Ї. Я«цЯ«┐Я«БЯ»ЇЯ««Я«еЯ«┐Я«▓Я»ѕ Я«фЯ»єЯ«░Я«┐Я«▓Я«┐Я«»Я««Я»Ї Я«ЋЯ»ЂЯ«│Я»ІЯ«░Я»ѕЯ«ЪЯ»Ђ, Я«ЋЯ»ѓЯ«░Я»ЇЯ««Я»ЂЯ«ЕЯ»ѕ Я«еЯ«ЙЯ«▒Я»ЇЯ«фЯ«ЪЯ»ЇЯ«ЪЯ«ЋЯ«цЯ»ЇЯ«цЯ»ѕЯ«фЯ»Ї Я«фЯ»єЯ«▒Я»ЇЯ«▒Я»ЂЯ«│Я»ЇЯ«│ Я«њЯ«░Я»Ђ Я«фЯ«░Я«┐Я««Я«ЙЯ«Е Я«фЯ«▓Я«фЯ«ЪЯ«┐Я«»Я«ЙЯ«ЋЯ»ЂЯ««Я»Ї[3] . Я«ЄЯ«цЯ«▒Я»ЇЯ«ЋЯ»Ђ Я«еЯ»ЄЯ«░Я»ЇЯ««Я«ЙЯ«▒Я«ЙЯ«Ћ Я«фЯ»єЯ«░Я«┐Я«▓Я«┐Я«»Я««Я»Ї Я«фЯ»ЂЯ«│Я»ІЯ«░Я»ѕЯ«ЪЯ»Ђ Я«јЯ«ЕЯ»ЇЯ«фЯ«цЯ»Ђ Я«фЯ«ЪЯ«┐Я«ЋЯ«ЋЯ»ЇЯ«ЋЯ«▓Я»Ї Я«хЯ«ЋЯ»ѕЯ«ЋЯ»Ї Я«ЋЯ«ЕЯ«┐Я««Я««Я»Ї Я«ЋЯ»ЂЯ«хЯ«ЙЯ«░Я»ЇЯ«ЪЯ»ЇЯ«џЯ»Ђ Я«фЯ»ІЯ«▓ Я«њЯ«░Я»Ђ Я««Я»ЂЯ«фЯ»ЇЯ«фЯ«░Я«┐Я««Я«ЙЯ«Е Я«фЯ«▓Я«фЯ«ЪЯ«┐Я«»Я«ЙЯ«ЋЯ»ЂЯ««Я»Ї. Я«хЯ«ЙЯ«»Я»Ђ Я«еЯ«┐Я«▓Я»ѕЯ«»Я«┐Я«▓Я»Ї Я«ЄЯ«цЯ»Ђ Я«еЯ»ЄЯ«░Я«┐Я«»Я«▓Я»Ї Я«њЯ«▒Я»ЇЯ«▒Я»ѕЯ«фЯ»ЇЯ«фЯ«ЪЯ«┐ Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї Я«ЄЯ«░Я«БЯ»ЇЯ«ЪЯ»Ђ Я«ЋЯ»ЂЯ«│Я»ІЯ«░Я«┐Я«ЕЯ»ЇЯ«ЋЯ«│Я»Ї Я«ЄЯ«БЯ»ѕЯ«еЯ»ЇЯ«ц Я«ЄЯ«БЯ»ѕЯ«фЯ»ЇЯ«фЯ»Ђ Я«ЄЯ«░Я«ЪЯ»ЇЯ«ЪЯ»ѕЯ«фЯ»ЇЯ«фЯ«ЪЯ«┐ Я«єЯ«ЋЯ«┐Я«» Я«ЄЯ«░Я«БЯ»ЇЯ«ЪЯ»Ђ Я«еЯ«┐Я«▓Я»ѕЯ«ЋЯ«│Я«┐Я«▓Я»ЂЯ««Я»Ї Я«ЋЯ«ЙЯ«БЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЂЯ«ЋЯ«┐Я«▒Я«цЯ»Ђ. Я«ЄЯ«ЎЯ»ЇЯ«ЋЯ»Ђ Я«фЯ»єЯ«░Я«┐Я«▓Я«┐Я«»Я««Я»Ї Я««Я»ѓЯ«ЕЯ»ЇЯ«▒Я»Ђ Я«єЯ«»Я«ЎЯ»ЇЯ«ЋЯ«│Я»ЂЯ«ЪЯ«ЕЯ»Ї Я«ЅЯ«│Я»ЇЯ«│Я«цЯ»Ђ[4] . Я«њЯ«▒Я»ЇЯ«▒Я»ѕЯ«фЯ»ЇЯ«фЯ«ЪЯ«┐Я«ЋЯ«│Я«┐Я«ЕЯ»Ї Я«еЯ»ЄЯ«░Я«┐Я«»Я«▓Я»Ї Я«хЯ«ЪЯ«┐Я«хЯ«цЯ»ЇЯ«цЯ»ѕ Я«хЯ«▓Я»ЂЯ«хЯ«│Я«хЯ»Ђ Я«ЊЯ«ЪЯ»ЇЯ«ЪЯ»Ђ Я«ЄЯ«▓Я«цЯ»ЇЯ«цЯ«┐Я«░Я«ЕЯ»Ї Я«џЯ»ІЯ«ЪЯ«┐Я«ЋЯ«│Я«┐Я«ЕЯ»Ї Я«цЯ«│Я»ЇЯ«│Я»ЂЯ«ЋЯ»ѕЯ«ЋЯ»Ї Я«ЋЯ»іЯ«│Я»ЇЯ«ЋЯ»ѕ Я««Я»ЂЯ«ЕЯ»ЇЯ«ЋЯ«БЯ«┐Я«цЯ»ЇЯ«цЯ»ЂЯ«ЋЯ»Ї Я«ЋЯ»ѓЯ«▒Я«┐Я«»Я«цЯ»Ђ. Я«ЄЯ«░Я«БЯ»ЇЯ«ЪЯ«ЙЯ«хЯ«цЯ»Ђ Я«цЯ»іЯ«ЋЯ»ЂЯ«цЯ«┐Я«»Я«┐Я«▓Я»Ї Я«ЅЯ«│Я»ЇЯ«│ Я«џЯ«┐Я«▓ Я«ЋЯ«Е Я«ЅЯ«▓Я»ІЯ«ЋЯ«ЎЯ»ЇЯ«ЋЯ«│Я«┐Я«ЕЯ»Ї Я«еЯ»ЄЯ«░Я«┐Я«»Я«▓Я»Ї Я«хЯ«ЪЯ«┐Я«хЯ«цЯ»ЇЯ«цЯ»ЂЯ«ЪЯ«ЕЯ»Ї Я«ЄЯ«цЯ»Ђ Я««Я«ЙЯ«▒Я»ЂЯ«фЯ«ЙЯ«ЪЯ»Ђ Я«ЋЯ»іЯ«БЯ»ЇЯ«ЪЯ»ЂЯ«│Я»ЇЯ«│Я«цЯ»Ђ. Я«ЅЯ«цЯ«ЙЯ«░Я«БЯ««Я«ЙЯ«Ћ CaF2 SrF2, BaF2, SrCl2, BaCl2, BaBr2, Я««Я«▒Я»ЇЯ«▒Я»ЂЯ««Я»Ї BaI2, Я«єЯ«ЋЯ«┐Я«»Я«Е Я«еЯ»ЄЯ«░Я«┐Я«»Я«▓Я»Ї Я«хЯ«ЪЯ«┐Я«хЯ««Я«┐Я«▓Я»ЇЯ«▓Я«ЙЯ«цЯ«хЯ»ѕ Я«єЯ«ЋЯ»ЂЯ««Я»Ї. Я«хЯ«┐Я«ЕЯ»ѕЯ«ЋЯ«│Я»ЇЯ«ЅЯ«▓Я«░Я»ЇЯ«еЯ»ЇЯ«ц Я«ЋЯ«ЙЯ«▒Я»ЇЯ«▒Я«┐Я«▓Я»Ї Я«фЯ»єЯ«░Я«┐Я«▓Я«┐Я«»Я««Я»Ї Я«ЋЯ»ЂЯ«│Я»ІЯ«░Я»ѕЯ«ЪЯ»Ђ Я«еЯ«┐Я«▓Я»ѕЯ«фЯ»ЇЯ«фЯ»ЂЯ«цЯ»ЇЯ«цЯ«ЕЯ»ЇЯ««Я»ѕЯ«»Я»ЂЯ«ЪЯ«ЕЯ»Ї Я«ЋЯ«ЙЯ«БЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЂЯ«ЋЯ«┐Я«▒Я«цЯ»Ђ. Я«ЄЯ«цЯ»ЂЯ«хЯ»іЯ«░Я»Ђ Я«ЄЯ«▓Я»ѓЯ«хЯ«┐Я«ЋЯ»ЇЯ«ЋЯ««Я«┐Я«▓Я««Я»Ї Я«јЯ«ЕЯ»ЇЯ«фЯ«цЯ«ЙЯ«▓Я»Ї Я«џЯ«┐Я«▓ Я«хЯ»ЄЯ«цЯ«┐ Я«хЯ«┐Я«ЕЯ»ѕЯ«ЋЯ«│Я«┐Я«▓Я»Ї Я«хЯ«┐Я«ЕЯ»ѕЯ«»Я»ѓЯ«ЋЯ»ЇЯ«ЋЯ«┐Я«»Я«ЙЯ«ЋЯ«фЯ»Ї Я«фЯ«»Я«ЕЯ»ЇЯ«фЯ«ЪЯ»ЂЯ«цЯ»ЇЯ«цЯ»ЂЯ«ЋЯ«┐Я«▒Я«ЙЯ«░Я»ЇЯ«ЋЯ«│Я»Ї. Я««Я»ЄЯ«▓Я»ЂЯ««Я»Ї Я«ЄЯ«цЯ»Ђ Я«еЯ»ђЯ«░Я«ЙЯ«▒Я»Ї Я«џЯ«┐Я«цЯ»ѕЯ«ЋЯ»ЇЯ«ЋЯ«фЯ»ЇЯ«фЯ«ЪЯ»ЇЯ«ЪЯ»Ђ Я«љЯ«цЯ«░Я«џЯ«ЕЯ»Ї Я«ЋЯ»ЂЯ«│Я»ІЯ«░Я»ѕЯ«ЪЯ«ЙЯ«Ћ Я««Я«ЙЯ«▒Я»ЂЯ«ЋЯ«┐Я«▒Я«цЯ»Ђ. BeCl2 + 2H2O Рєњ Be(OH)2 + 2 HCl Я«ЄЯ«џЯ»ЇЯ«џЯ»ЄЯ«░Я»ЇЯ««Я««Я»Ї Я«еЯ«ЙЯ«ЕЯ»ЇЯ«« Я«љЯ«цЯ«░Я»ЄЯ«ЪЯ»ЇЯ«ЪЯ«ЙЯ«ЋЯ«хЯ»ЂЯ««Я»Ї Я«ЅЯ«░Я»ЂЯ«хЯ«ЙЯ«ЋЯ«┐Я«▒Я«цЯ»Ђ.BeCl2Рђб4H2O ([Be(H2O)4]Cl2). BeCl2 Я«єЯ«ЋЯ»ЇЯ«џЯ«┐Я«џЯ«ЕЯ»ЄЯ«▒Я«┐Я«» Я«ЋЯ«░Я»ѕЯ«фЯ»ЇЯ«фЯ«ЙЯ«ЕЯ«ЙЯ«Е Я«ѕЯ«цЯ«░Я«┐Я«▓Я»Ї Я«ЋЯ«░Я»ѕЯ«ЋЯ«┐Я«▒Я«цЯ»Ђ.[5][6] Я«фЯ«»Я«ЕЯ»ЇЯ«ЋЯ«│Я»ЇЯ««Я«┐Я«ЕЯ»ЇЯ«ЕЯ«ЙЯ«▒Я»ЇЯ«фЯ«ЋЯ»ЂЯ«фЯ»ЇЯ«фЯ»Ђ Я««Я»ЂЯ«▒Я»ѕЯ«»Я«┐Я«▓Я»Ї Я«фЯ»єЯ«░Я«┐Я«▓Я«┐Я«»Я««Я»Ї Я«цЯ«»Я«ЙЯ«░Я«┐Я«фЯ»ЇЯ«фЯ«цЯ«▒Я»ЇЯ«ЋЯ»Ђ Я«фЯ»єЯ«░Я«┐Я«▓Я«┐Я«»Я««Я»Ї Я«ЋЯ»ЂЯ«│Я»ІЯ«░Я»ѕЯ«ЪЯ»Ђ Я««Я»ѓЯ«▓Я«фЯ»ЇЯ«фЯ»іЯ«░Я»ЂЯ«│Я«ЙЯ«Ћ Я«ЅЯ«│Я»ЇЯ«│Я«цЯ»Ђ. Я«фЯ«┐Я«░Я»ђЯ«ЪЯ«▓Я»Ї Я«ЋЯ«┐Я«░Я«ЙЯ«фЯ»ЇЯ«ЪЯ»ЇЯ«џЯ»Ђ Я«хЯ«┐Я«ЕЯ»ѕЯ«»Я«┐Я«ЕЯ»Ї Я«фЯ»іЯ«┤Я»ЂЯ«цЯ»Ђ Я«ЄЯ«цЯ»Ђ Я«хЯ«┐Я«ЕЯ»ѕЯ«»Я»ѓЯ«ЋЯ»ЇЯ«ЋЯ«┐Я«»Я«ЙЯ«ЋЯ«фЯ»Ї Я«фЯ«»Я«ЕЯ»ЇЯ«фЯ«ЪЯ»ЂЯ«ЋЯ«┐Я«▒Я«цЯ»Ђ. Я««Я»ЄЯ«▒Я»ЇЯ«ЋЯ»ІЯ«│Я»ЇЯ«ЋЯ«│Я»Ї
Я«хЯ»єЯ«│Я«┐ Я«ЄЯ«БЯ»ѕЯ«фЯ»ЇЯ«фЯ»ЂЯ«ЋЯ«│Я»Ї
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Portal di Ensiklopedia Dunia