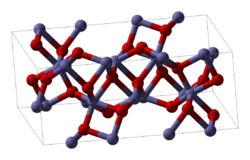
ரோடியம்(III) ஆக்சைடு
ரோடியம்(III) ஆக்சைடு அல்லது ரோடியம் செசுகியுவாக்சைடு (Rhodium(III) oxide or Rhodium sesquioxide) என்பது Rh2O3 என்ற மூலக்கூற்று வாய்ப்பாடு கொண்ட ஒரு கனிம வேதியியல் சேர்மமாகும். அமைப்புRh2O3 பிரதானமாக இரண்டு படிக வடிவங்களில் காணப்படுகிறது. அறுகோண வடிவ ரோடியம்(III) ஆக்சைடு குருந்தக்கல் அமைப்பில் உள்ளது, இப்படிகம் 750°செ வெப்பநிலைக்குச் சூடுபடுத்தும்போது செஞ்சாய்சதுரப் படிக அமைப்பிற்கு நிலை மாறுகிறது[1]. தயாரிப்புரோடியம்(III) ஆக்சைடை பலவழி முறைகளில் தயாரிக்கலாம். ரோடியம் உலோகத் தூளானது பொட்டாசியம் ஐதரசன் சல்பேட்டுடன் சேர்த்து உருக்கப்பட்டு, இதனுடன் சோடியம் ஐதராக்சைடு சேர்க்கப்படுகிறது. இதன் விளைவாக ரோடியம்(III) ஆக்சைடின் நீரேற்று வடிவம் உருவாகிறது. மேலும் இதைச் சூடாக்கினால் ரோடியம்(III) ஆக்சைடு கிடைக்கிறது[2].
இயற்பியல் பண்புகள்ரோடியம் ஆக்சைடு படலங்கள் , வேகமான ஒர் இரு வகை மின்வண்ண அமைப்புகளாக நடந்துகொள்கின்றன: மீளும் மஞ்சள்↔ அடர் பச்சை அல்லது மஞ்சள் ↔ பழுப்பு – கருஞ்சிவப்பு வண்ண மாற்றங்கள் அடர் மஞ்சள் ↔ பழுப்பு ஊதா நிற மாற்றங்கள் ~1 V மின்னழுத்தத்தைச் செலுத்தும் போது KOH கரைசல்களில் பெறப்படுகின்றன[5] ரோடியம் ஆக்சைடு படலங்கள், பொதுவான ஒளிஊடுறுவும் மின்முனையான இண்டியம் வெள்ளீயம் ஆக்சைடு (ITO) படலங்கள் போன்று ஒளிபுகும் தன்மையுடனும் மின்கடத்தும் தன்மையும் கொண்டு உள்ளன. ஆனால் Rh2O3 0.2 eV அளவிற்கு இண்டியம் வெள்ளீயம் ஆக்சைடை விட வேலைத்திறன் குறைவாக உள்ளது. இதன் விளைவாக, இண்டியம் வெள்ளீயம் ஆக்சைடு மீது ரோடியம் ஆக்சைடு படிவை ஏற்படுத்தி அதன் மூலம் கரிம ஒளி உமிழும் டையோடுகளின் மின் பண்புகளை மேம்படுத்தலாம்[3]. பயன்கள்வினையூக்கியாகச் செயல்படுவதுதான் ரோடியம் ஆக்சைடின் பிரதானமான பயனாகும். உதாரணமாக CO[6] அல்லது NO[7] வாயுக்களாக மாற்றும் செயல். பாதுகாப்புஅதிக வெப்பம், கரிமக் கரைப்பான்கள், ஐதரோகுளோரிக் அமிலம், ஐதரோகந்தக அமிலம் மற்றும் அமோனியா போன்ற வேதிப்பொருட்களிடம் இருந்து ரோடியம் ஆக்சைடு தவிர்க்கப்பட வேண்டும். மேலும் காண்கமேற்கோள்கள்
|
||||||||||||||||||||||||||||||||||||||||||||
Portal di Ensiklopedia Dunia